��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �ı������������Ӱ�컯ѧ��Ӧ���ʣ��Է�ӦH2(g)+I2(g)  2HI(g)��������ʹ����Ӱٷ������ӵ��ǣ���������ϵ���¶� �����ӷ�Ӧ��Ũ�� �����������ѹǿ ��ʹ�ô���
2HI(g)��������ʹ����Ӱٷ������ӵ��ǣ���������ϵ���¶� �����ӷ�Ӧ��Ũ�� �����������ѹǿ ��ʹ�ô���
A���٢�
B���٢�
C���ڢ�
D���ۢ�
�ο��𰸣�B
���������
����������١������¶ȣ�����Ӱٷ������࣬��ȷ�������ӷ�Ӧ��Ũ�Ⱦ������˵�λ����Ļ���ӵ���Ŀ���Ӷ�������Ч��ײ����Ӧ�������ӣ�������Ӱٷ����Dz���� �����۶������������Ļ�ѧ��Ӧ��������������ʱ���������������ѹǿ���������С����Ӧ��Ũ������λ����ڻ���������࣬�� ����Ӱٷ����Dz���ģ����ܴ����ı仯ѧ��Ӧ�����ǽ����˷�Ӧ�Ļ�ܣ�����Ӱٷ������࣬��ȷ��ѡB��
���㣺���黯ѧ��Ӧ������ת����ԭ��
�����Ѷȣ�һ��
2������� ���ܱ������з������з�Ӧ��I2(g)+H2(g)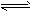 2HI(g)(����Ӧ����) ��ʼʱ��n(H2)=a mol��n(I2)=b mol��ֻ�ı�����г��������������������䣬�Խ���ѧ��Ӧ���ʵĸı�(��������С�����䡱)������Ӧ�ı���
2HI(g)(����Ӧ����) ��ʼʱ��n(H2)=a mol��n(I2)=b mol��ֻ�ı�����г��������������������䣬�Խ���ѧ��Ӧ���ʵĸı�(��������С�����䡱)������Ӧ�ı���

�ο��𰸣���1������
��2������
��3������
��4��
���������
�����Ѷȣ�һ��
3������� ijͬѧ����ϡ����������ȡ������ʵ���У����ּ��������Ȼ�ͭ��Һ�ɼӿ��������������ʣ���ش��������⣺
��1��Ҫ�ӿ�����ʵ����������������ʣ����ɲ�ȡ�Ĵ�ʩ��______��______�������֣���
��2��ʵ����������NaCl��CuSO4��FeCl2��ZnCl2��4����Һ������ʵ����CuCl2��Һ���������õ���______��
��3��Ϊ�˽�һ���о��Ȼ�ͭ�����������������ʵ�Ӱ�죬��ͬѧ���������һϵ��ʵ�飮�����������Ļ����Һ�ֱ���뵽6��ʢ�й���Zn���ķ�Ӧƿ�У��ռ����������壬��¼�����ͬ�������������ʱ�䣮
| ʵ�飨�����Һ�� | ????A | ????B | ????C | ????D | ????E | ????F
4mol/L??����/mL
???60
???V1
????V2
????V3
???V4
???V5
����CuCl2��Һ/mL
????0
???1.0
????5.0
???10
???V6
???40
H2O/mL
???V7
???V8
???V9
???V10
???20
????0
������ɴ�ʵ����ƣ����У�V1=______��V6=______��V9=______��
�ڸ�ͬѧ���ó��Ľ���Ϊ������������CuCl2��Һʱ���������������ʻ�����ߣ����������CuCl2��Һ����һ����ʱ���������������ʷ������½���
������������������½�����Ҫԭ��______��
�ο��𰸣���1���������¶ȡ��ʵ���������Ũ�ȡ�����Zn�ĽӴ�����ɼӿ�
���������
�����Ѷȣ�һ��
4��ѡ���� ���������ҹ���������п��a��b�зֱ������ͬ�������ͬ���ʵ���Ũ�ȵ�ϡ���ᣬͬʱ��a�м�����������ͭ��Һ�����и�ͼ����H2�����V��L����ʱ��t��min���Ĺ�ϵ����ȷ���ǣ�������
A��
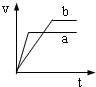
B��
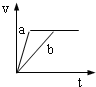
C��
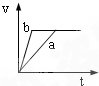
D��
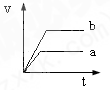
�ο��𰸣��������֪����Ӧ������Zn+2H+�TZn2++H2����Zn��
���������
�����Ѷȣ���
5��ѡ���� ������ѧ��Ӧ���ʵ���Ҫԭ����[???? ]
A���μӷ�Ӧ�ﱾ��������
B���������
C���¶Ⱥ�ѹǿ
D������Ӧ����������Ũ��
�ο��𰸣�A
���������
�����Ѷȣ���
|