微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质中,属于共价化合物的是
A.NH4Cl
B.H2SO4
C.NaCl
D.I2
参考答案:B
本题解析:共价化合物只含有共价键,大都有不同的非金属元素组成,个别如AlCl3也为共价化合物,但由非金属性元素组成的化合物不一定为共价化合物,也可能为离子化合物,如铵盐.
解答:解:A.NH4Cl为离子化合物,不是共价化合物,故A错误;
B.H2SO4为共价化合物,只含有共价键,故B正确;
C.NaCl为离子化合物,故C错误;
D.I2为单质,不是化合物,故D错误.
故选B.
本题难度:困难
2、选择题 只用试管和胶头滴管就可以对下列各组中的两种溶液进行鉴别的是
①AlCl3溶液和NaOH溶液???? ②Ca(HCO3)2溶液和NaOH溶液???? ③Na[Al(OH)4]溶液和盐酸??
④Al2(SO4)3溶液和氨水????⑤Ag(NO3)2溶液和氨水.
A.①③⑤
B.①②③
C.②③④
D.③④⑤
参考答案:A
本题解析:分析:只要用试管和胶头滴管,不用任何化学试剂就可以鉴别的物质可以采用相互滴加的方法检验,滴加顺序不同,现象不同的可以鉴别.
解答:①将氯化铝溶液滴加到氢氧化钠溶液中先没有现象,后生成沉淀,将氢氧化钠滴到氯化铝溶液中先生成沉淀后沉淀消失,二者现象不同,可鉴别,故正确;
②无论将Ca(HCO3)2溶液滴到NaOH溶液中还是将氢氧化钠溶液滴到碳酸氢钙溶液中,都生成白色沉淀,现象相同,不能鉴别,故错误;????
③将Na[Al(OH)4]溶液滴到盐酸中先没有现象,后生成沉淀,将盐酸滴到Na[Al(OH)4]溶液中先生成沉淀后沉淀消失,二者现象不同,可鉴别,故正确;
④无论将Al2(SO4)3溶液滴到氨水中还是将氨水滴到硫酸铝溶液中都生成白色沉淀,现象相同,不能鉴别,故错误;????
⑤将Ag(NO3)2溶液滴到氨水中先没有现象后生成沉淀,将氨水滴到硝酸银溶液中先生成沉淀后沉淀消失.二者现象不同,可以鉴别,故正确.
故选A.
点评:本题考查不加任何试剂的鉴别,题目难度中等,注意物质发生反应的现象,牢固掌握相关基础知识,是解答此类题目的关键.
本题难度:一般
3、选择题 某有机物含有C、H、O、N等元素,该有机物在水中形成的分散系无丁达尔效应,则该有机物可能是
A.脂肪
B.淀粉
C.蛋白质
D.氨基酸
参考答案:D
本题解析:
本题难度:一般
4、选择题 X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是
A.元素Y、Z、W离子具有相同的电子层结构,其半径依次增大
B.元素X与元素Y可以形成两种共价化合物,且这两种化合物只有一种类型的共价键
C.元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR
D.元素W、R的最高价氧化物对应水化物都是强酸
参考答案:C
本题解析:试题分析:X是周期表中原子半径最小的元素,应为H元素。Y原子最外层电子数是次外层电子数的3倍,应为O元素。根据Z、W、R处于同一周期,R与Y处于同一族,则R为S元素;Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等,则Z、W原子的核外电子数之和为8+16=24。又Z、W、处于同一周期,应为第三周期,分别为Na和Al元素。
A、从题目所给的条件可以看出X是H元素,Y是O元素,Z是Na元素,W是Al元素,R是S元素.Y、Z、W具有相同电子层结构的离子(O2-、Na+、Al3+),根据核外电子排布相同的微粒,半径随着核电荷数的增加而减小,其半径依次减小,故A错误;
B、X和Y元素能形成2种化合物,X2Y(H2O)和X2Y2(H2O2),其中双氧水中含有极性键和非极性键,故B错误;
C、元素Y、R分别与元素X形成的化合物是氢化物,因为Y(O元素)和R(S元素)的非金属性强弱:Y>R,所以对应的氢化物的稳定性:XmY>XmR,故C正确;
D、W元素最高价氧化物的水化物是Mg(OH)2,是中强碱,而R元素最高价氧化物的水化物是H2SO4,是强酸,故D错误,答案选C。
考点:考查元素周期表的结构和元素周期律的应用
点评:该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。做题时注意以下问题:①同周期、同主族内元素性质(核外电子排布、原子半径、金属性、非金属性、酸碱性、气态氢化物的热稳定性等)变化规律。②元素之间化合所形成化合物的化学式的书写。
本题难度:简单
5、选择题 下列化合物的电子式正确的是
A.H:Cl
B.[:Cl:]- Ca+2[:Cl:]-
C.Ca2+[:Cl:]2-
D.H : O:O: H
参考答案:D
本题解析:氯化氢是共价化合物,氯原子还有没有参与成键但电子,正确的电子式为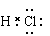 。氯化钙是离子化合物,B中所带电荷数书写错误的,C中阴离子不能合并,正确的为
。氯化钙是离子化合物,B中所带电荷数书写错误的,C中阴离子不能合并,正确的为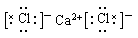 。所以答案是D。
。所以答案是D。
本题难度:困难