微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法完全正确的是 (?? )
A.放热反应均是自发反应
B.ΔS 为正值的反应均是自发反应
C.物质的量增加的反应,ΔS为正值
D.如果ΔH和ΔS 均为正值,当温度升高时,反应可能自发进行
参考答案:D
本题解析:只有满足△G=△H-T・△S<0,反应才能是自发的,所以A、B都是不一定自发,不正确。熵是与物质的状态有关系的,同一种物质在气态熵值增大,液态其次,固态最小,所以C也是错误的。所以选项D是正确的。答案选D。
本题难度:一般
2、选择题 已知:体系的自由能变化ΔG=ΔH-TΔS<0时,反应能自发进行。下列反应中,一定不能自发进行的是( )
A.2KClO3(s)=2KCl(s)+3O2(g) ΔH=-78.03kJ/mol ΔS="1110" J/(mol・K)
B.CO(g)=C(s,石墨)+1/2O2(g) ΔH=110.5kJ/mol ΔS="-89.36" J/(mol・K)
C.4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s) ΔH=-444.3kJ/molΔS="-280.1" J/(mol・K)
D.NH4HCO3(s)+CH3COOH(aq)=CO2(g)+CH3COONH4(aq)+H2O(l)
ΔH=37.301kJ/mol ??? ΔS="184.05" J/(mol・K)
参考答案:B
本题解析:
试题分析:体系的自由能变化ΔG=ΔH-TΔS<0时,反应能自发进行。根据以上已知条件计算ΔH-TΔS判断是否小于零,即可判断反应是否自发。故本题答案选B。
点评:本题考查化学反应进行的方向,题目难度不大,可根据题意进行解答。
本题难度:简单
3、选择题 光谱研究表明,易溶于水的S02所形成的溶液中存在着下列平衡:据此,下列判断中正确的是( )
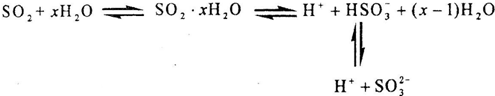
A.该溶液中存在着SO2分子
B.该溶液中H+浓度是SO32-浓度的2倍
C.向该溶液中加入足量的酸都能放出SO2气体
D.向该溶液中加入过量NaOH可得到Na2SO3、NaHSO3和NaOH的混合溶液
参考答案:A、因为该反应是可逆反应,所以达到平衡后反应物和生成物共同存
本题解析:
本题难度:简单
4、选择题 恒温恒压,反应A+B=C+D,在下列哪种情况下,一定能自发进行
A.△H<0 △S>0
B.△H>0 △S>0
C.△H<0 △S<0
D.△H>0 △S<0
参考答案:A
本题解析:
试题分析:自发进行的反应△G <0, △G=△H-T△S,A.△H<0 △S>0,则△G <0,反应自发进行,B.△H>0 △S>0 ,△G不能确定;C.△H<0 △S<0 △G不能确定;D.△H>0 △S<0 ,△G>0,反应不能自发进行。选A。
考点:反应自发性的判断。
本题难度:一般
5、选择题 已知“凡气体分子总数增多的反应一定是熵增大的反应”。一定条件下,下列反应不可能自发进行的是[???? ]
A. 2O3 (g)==3O2 (g) △H<0
B. 2CO(g)==2C(s)+O2 (g) △H>0
C. N2(g)+3H2 (g)==2NH3 (g) △H<0
D. CaCO3 (s)==CaO(s)+CO2 (g) △H>0
参考答案:B
本题解析:
本题难度:一般