微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是
A.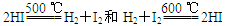 是可逆反应
是可逆反应
B.在可逆反应中,使用催化剂可以同等程度的改变正、逆反应速率
C.任何可逆反应的反应限度都相同
D.在可逆反应中,使用催化剂会增大正反应速率,减小逆反应速率
参考答案:B
本题解析:A中反应条件不同,不是可逆反应。影响限度的主要因素是物质的性质,C不正确。催化剂能够同等程度改变正逆反应速率,所以B正确,D不正确。答案选B。
本题难度:一般
2、选择题 500 mL 1 mol/L的稀HCl与锌粒反应,不会使反应速率加快的是
A.升高温度
B.将500 mL 1 mol/L的HCl改为1000 mL 1 mol/L的HCl
C.用1 mol/L的H2SO4代替1 mol/L的HCl
D.用锌粉代替锌粒
参考答案:B
本题解析:
试题分析:温度越高,反应速率越快,故A错误;500 mL 1 mol/L的HCl改为1000 mL 1 mol/L的HCl,H+浓度不变,反应速率不变,故B正确;1 mol/L的H2SO4代替1 mol/L的HCl,H+浓度增大,反应速率加快,故B错误;锌粉代替锌粒,增大反应物接触面积,反应速率加快,故D错误。
考点:本题考查化学反应速率。
本题难度:一般
3、填空题 17.⑴(9分)已知2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10 ,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
①请写出方框内物质的化学式: 。
②针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是 的影响。
③若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是 。
A.硫酸钾
B.硫酸锰
C.水
D.氯化锰
参考答案:CO2;催化剂;B
本题解析:
试题分析:根据原子守恒,反应物含O原子40个,C原子10个,反应后产物即为10CO2;KMnO4与H2C2O4反应生成硫酸锰,锰离子有催化作用,所以猜想可能是催化剂的作用;要想验证锰离子的催化作用,在做对比实验时同时加入硫酸锰观察反应速率是否变化即可。
考点:氧化还原反应方程式的配平、化学反应速率的影响因素
点评:本题考察了氧化还原反应的配平及影响反应速率的因素,难度较小,要把握质量守恒定律的应用。
本题难度:一般
4、选择题 用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加快的是( )
A.滴加少量CuSO4溶液
B.不用稀硫酸,改用98%的浓硫酸
C.对该反应体系加热
D.不用铁片,改用铁粉
参考答案:A、滴加少量CuSO4溶液,铁置换出Cu,构成Fe、Cu原电
本题解析:
本题难度:一般
5、选择题 铝与过量的稀盐酸反应,为了加快反应速率,但是又不影响生成的氢气总量,可以采取的措施是(??)
A.加入适量的铝粉
B.加入适量的水
C.加入少量的硫酸铜溶液
D.加入浓度较大的盐酸
参考答案:D
本题解析:考查外界条件对反应速率的影响。铝粉的接触面积大,反应速率大,但产生的氢气也多,A不正确。B是降低氢离子浓度,反应速率降低。C中会消耗铝,生成氢气偏少,不正确。答案选D。
本题难度:简单