微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 香烟烟雾中含有CO、CO2、SO2、H2O等气体.用a.无水硫酸铜b.澄清石灰水c.红热氧化铜d.生石灰e.品红溶液等可将其一一检出,检出的正确顺序是( )
A.混合气→a→e→e→b→d→c
B.混合气→c→d→e→e→a
C.混合气→a→e→b→a→d→c
D.混合气→b→e→a→d→c
2、选择题 某地污水中含有Zn2+、Hg2+、Fe3+和Cu2+四种阳离子。甲、乙、丙三位同学设计的从该污水中回收金属铜的方案如下
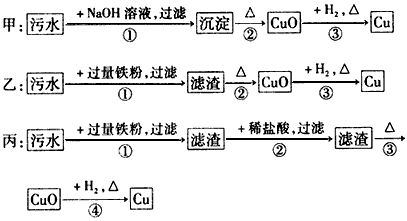
下列判断正确的是[???? ]
A.三种实验方案中都能制得纯净的铜
B.乙方案中加过量铁粉可以将四种阳离子全部还原
C.甲方案中的反应涉及置换、分解、化合、复分解四种反应类型
D.丙方案会产生环境污染
3、简答题 肉桂酸主要用于制备酯类,还用作植物生长促进剂、长效杀菌剂.苯甲醛和乙酸酐在碱性催化剂(如无水K2CO3)作用下,生成肉桂酸,方程式如下:
C6H5CHO+(CH3CO)2O?C6H5CH=CHCOOH+CH3COOH
有关数据如下表: