��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1�������� ��8�֣�200��ʱ��11��6gCO2��ˮ�����Ļ��������������Na2O2��?�ַ�Ӧ���������������3��6g����ͼ��ʾ������ԭ�������CO2��H2O�����ʵ����ȡ�
�ο��𰸣�CO2��H2O�����ʵ�����1��4
�������������Ӧ�ù������Ʒ�Ӧ���йؼ��㡣
��ԭ�������CO2��H2O�����ʵ����ֱ�Ϊ mol��
mol�� mol
mol
2Na2O
�����Ѷȣ�һ��
2��ѡ���� ����������ΪN��R2+���ӣ�������ΪA����n g �������������������ӵ����ʵ���Ϊ��??��
A��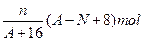
B��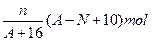
C��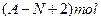
D��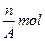
�ο��𰸣�
�����������
�����Ѷȣ���
3��ѡ���� ��״�����Т�6.72L�����3.01��1023���Ȼ�����Ӣ�13.6 g�����0.2 mol NH3�����ж�����������Ĺ�ϵ��С�����ʾ����ȷ����
A���������<��<��<��
B���ܶȣ���<��<��<��
C����������<��<��<��
D����ԭ��������<��<��<��
�ο��𰸣�A
���������
�����������6.72L CH4���ʵ���Ϊ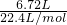 =0.3mol����3.01��1023��HCl���ӵ����ʵ���Ϊ0.5mol����13.6g H2S �����ʵ���Ϊ
=0.3mol����3.01��1023��HCl���ӵ����ʵ���Ϊ0.5mol����13.6g H2S �����ʵ���Ϊ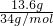 =0.4mol����0.2mol NH3����ͬ�����£���������֮�ȵ������ʵ���֮�ȣ���������ڣ��ۣ��٣��ܣ�A�������ʵ�Ħ�������ֱ�Ϊ��CH4Ϊ16g/mol��HClΪ36.5g/mol ��H2S Ϊ34g/mol��NH3Ϊ17g/mol����ͬ�����£��ܶ�֮�ȵ���Ħ������֮�ȣ������ܶȢڣ��ۣ��ܣ��٣�B��ȷ�������ʵ������ֱ�Ϊ��CH4Ϊ0.3mol��16g/mol=4.8g��HClΪ0.5mol��36.5g/mol="33.25g" ��H2S 13.6g��NH3Ϊ0.2mol��17g/mol=3.4g�����������ڣ��ۣ��٣��ܣ�C��ȷ����������Hԭ�ӵ����ʵ����ֱ�Ϊ��CH4Ϊ0.3mol��4=1.2mol��HClΪ0.5mol��H2S 0.4mol��2=0.8mol��NH3Ϊ0.2mol��3=0.6mol��������ԭ�Ӹ����٣��ۣ��ܣ��ڣ�D��ȷ��ѡA��
=0.4mol����0.2mol NH3����ͬ�����£���������֮�ȵ������ʵ���֮�ȣ���������ڣ��ۣ��٣��ܣ�A�������ʵ�Ħ�������ֱ�Ϊ��CH4Ϊ16g/mol��HClΪ36.5g/mol ��H2S Ϊ34g/mol��NH3Ϊ17g/mol����ͬ�����£��ܶ�֮�ȵ���Ħ������֮�ȣ������ܶȢڣ��ۣ��ܣ��٣�B��ȷ�������ʵ������ֱ�Ϊ��CH4Ϊ0.3mol��16g/mol=4.8g��HClΪ0.5mol��36.5g/mol="33.25g" ��H2S 13.6g��NH3Ϊ0.2mol��17g/mol=3.4g�����������ڣ��ۣ��٣��ܣ�C��ȷ����������Hԭ�ӵ����ʵ����ֱ�Ϊ��CH4Ϊ0.3mol��4=1.2mol��HClΪ0.5mol��H2S 0.4mol��2=0.8mol��NH3Ϊ0.2mol��3=0.6mol��������ԭ�Ӹ����٣��ۣ��ܣ��ڣ�D��ȷ��ѡA��
���㣺���鳣�û�ѧ�����йؼ��㡢����٤�����ɼ����ۡ�
�����Ѷȣ�һ��
4�������� ��ͼװ���У��������ڳ���0.1 mol NO���壬�������װ��һ����Na2O2����A������ͨ��CO2���壮�����£��������л���������D�����ƶ���������C��ʱ���������С����С��Ϊԭ�����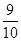 ������CO2�ļ���ͨ�룬�������������ƶ����������ǻ�����ĥ����
������CO2�ļ���ͨ�룬�������������ƶ����������ǻ�����ĥ����
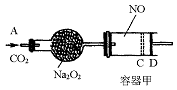
��֪�� 2Na2O2 + 2CO2 ��? 2Na2CO3 + O2
��1����֪����������C��ʱ������������ʵ�����������2.24 g��
�ٴ�ʱ��ͨ���״���µ�CO2�������L��
����������NO2ת��ΪN2O4��ת�����Ƕ��٣�
�ۻ�������C������ͨ��a mol CO2����ʱ����ǡ�û���D������aֵ��????0.01������ڡ�С�ڡ����ڣ�����������??????????????????????????????????��
��2�����ı�������Na2O2������Ҫͨ�����ڼ��������¶ȼ�ͨ�����CO2��ʹ����������D��C���ִ�C��D���ƶ�����Na2O2��������СֵӦ����________g��
�ο��𰸣�(��16��)
��1����CO2���1.792 L����3��
���������
���������
��1������ͨ���״����CO2��������Ϊx���������������Ϊy
2Na2O2+2CO2=Na2CO3+O2????? ��m��
2��22.4 L??????????22.4 L????? 56 g
x??????y????? 2.24 g
56 g�Ux��2��22.4 L��2.24 g
���x=1.792L��y=0.896L
n��O2��=0.04mol
2NO+ O2=2NO2
2??? 1??? 2
0.08 mol?0.04
�����Ѷȣ�һ��
5��ѡ���� ��FeCl3��CuCl2�Ļ����Һ�У��������Fe�ۣ���ȫ��Ӧ�����¹��������������Fe��������ȣ���ԭ���Һ��FeCl3��CuCl2�����ʵ���Ũ��֮��Ϊ?????????��???��
A��7��2
B��2��7
C��1��2
D��2��1
�ο��𰸣�B
������������Һ��FeCl3��CuCl2�����ʵ���Ũ��֮��=���ʵ���֮�ȣ���FeCl3�����ʵ���ΪX��CuCl2�����ʵ���ΪY������������Fe3+��Cu2+��Fe����FeCl3��Ӧ����FeCl3��Ӧ���Fe����CuCl2��Ӧ��
2FeCL3? +? Fe? =? 3FeCL2????����������С
X????????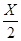 �����Ѷȣ���
�����Ѷȣ���