��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��Ϊ�˳�ȥKCl��Һ��������Mg2����SO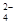 ����ѡ��Ba(OH)2��HCl��K2CO3�����Լ��������²��������
����ѡ��Ba(OH)2��HCl��K2CO3�����Լ��������²��������
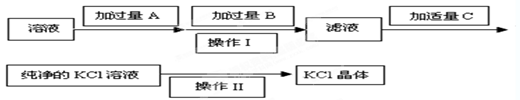
��1�������Լ��У� B��?????????��C��?????????��
(2)�������������??????????��
(3)�ӹ���Aʱ�����йط�Ӧ�����ӷ���ʽΪ ???????????????��??????????????????��
��һ����ɫϡ��Һ�п��ܺ���Na+��Fe3+��H+��Mg2����CO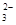 ?��OH����HCO
?��OH����HCO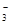 ��Cl���������е������֡�Ϊ��ȷ����Һ����ɣ����������²�����
��Cl���������е������֡�Ϊ��ȷ����Һ����ɣ����������²�����
����ʯ����ֽ����Һ������ԣ���ֽ����ɫ��
��ȡ2������Һ���ȼ�����ϡ�����ữ��������������ټ��Ȼ�����Һ���м��飬û����������
��1��ԭ��Һ��һ�����ڵ�������????????????????????????????????????????��һ�������ڵ�������??????????????????????????????????��
��2�������������������ܿ϶��Ƿ���ڵ�������??????????���������һ����ʵ�鷽�����ж��Ƿ�����������ӡ�??????????????????????????????????????
�ο��𰸣���(1)K2CO3��1�֣��� HCl��1�֣���??? (2)
���������
���������
��(1�������������Խ�MgCl2��MgSO4�е����������������ȥ������ʱ��ÿһ�����ӵ��Լ����ǹ����ģ�������������������̼��س�ȥ���������̼���������������ȥ�����Լ�A��B��C������Ba��OH��2��K2CO3��HCl��
��2��Һ��������ķ����ǹ��ˣ����ò���������©�������������ձ������ʵ���Һ��þ���ķ����������ᾧ��
��3�������������Խ�MgCl2��MgSO4�е����������������ȥ������ʽ�ֱ�Ϊ��MgCl2+Ba��OH��2�TBaCl2+Mg��OH��2����
�����Ѷȣ�һ��
2��ѡ���� ij��Һ�к��д�����Al3+��NH4+��Ag+��Fe2+�������ӡ������Һ�м�������Na2O2���Ȳ���ֽ�����ټ������ϡ���ᣬ��ʱ��Һ�д������ڵ������ӿ�����
A.Na+��NH4+��Al3+��H+
B.Fe2+��Al3+��Na+��H+
C.Na+��Fe3+��Al3+��H+
D.Ag+��Fe3+��Na+��H+
�ο��𰸣�C
���������
�����Ѷȣ�����
3��ѡ���� ������[KAl(SO4)2?12H2O]��Һ�еμ�Ba(OH)2��Һ����SO42-��ȫ����ʱ����Ԫ�صĴ�����ʽ�� ��???��????
A��ȫ��ΪAl(OH)3����
B������ȫ����[Al(OH)4]-��ʽ��������Һ��
C��һ����ΪAl(OH)3������һ������Al3����������Һ��
D��һ����ΪAl(OH)3������һ������[Al(OH)4]-��ʽ��������Һ��
�ο��𰸣�B
���������
���������4��2?12H2O��������Ϊ1mol������Һ�к���1molAl3+��2molSO42-���ɷ�ӦSO42-+Ba2+=BaSO4����֪��ʹSO42-ȫ��ת����BaSO4��������Ҫ2molBa��OH��2�������4molOH-������Al3++4OH-=[Al(OH)4]-�����������Һ�д���[Al(OH)4]-������������[KAl(SO4)2?12H2O]��Һ�еμ�Ba(OH)2��Һ����SO42-��ȫ����ʱ����Ԫ�صĴ�����ʽ�Ǽ���ȫ����[Al(OH)4]-��ʽ��������Һ�У��ʱ���Ĵ�ѡ��B
�����Ѷȣ�һ��
4��ѡ���� �ں������и����������Һ�У��ܴ�����������ҺΪ��ɫ������
A.Na+��Cu2+��Cl-��SO42-
B.Ba2+��K+��OH-��NO3-
C.K+��Ca2+��NH4+��CO32-
D.H+��Ca2+��Cl-��HCO3-
�ο��𰸣�B
�����������������������֮�䲻�ܽ�����ɳ��������塢ˮ�ȣ����ܴ������棬��������ӵ���ɫ�����
���A����������֮�䲻��Ӧ���ܹ��棬��Cu2+Ϊ��ɫ������ɫ��Һ��������A����
B����������֮�䲻��Ӧ���ܹ��棬�Ҿ�Ϊ��ɫ����B��ȷ��
C����Ca2+��CO32-������ɳ��������ܹ��棬��C����
D����H+��HCO3-�������ˮ�����壬���ܹ��棬��D����
��ѡB��
���������⿼�����ӵĹ��棬��Ϥ���ֽⷴӦ���������������ӵ���ɫ���ɽ����Ŀ�ϼ�
�����Ѷȣ�һ��
5��ѡ���� ij��Һ�к���HCO3����CO32����SO32����Na+��NO3���������ӡ��������м���Na2O2��ĩ����ַ�Ӧ����Һ����仯���Բ��ƣ�����Һ������Ũ�ȱ��ֲ������
A.NO3��
B.CO32����NO3��
C.SO32����NO3��
D.CO32����NO3����Na+
�ο��𰸣�A
������������������������������ˮ�����������ƺ������������������ܺ�HCO3����Ӧ����CO32��������������ƻ�����ǿ�����ԣ��ܰ�SO32����������SO42��������Ũ�Ȼ����������NO3������ѡA��
���㣺����������Ƶ����ʡ����ӹ�����й��ж�
���������������е��Ѷȵ����⣬�����״�ѡC����������ֻ���ǵ�������������ˮ�����������ƣ������Թ������Ƶ���һ����Ҫ���ʡ���ǿ�����Ե��µģ���˼�Ҫ���ջ���֪ʶ������Ҫ�����������֪ʶ��
�����Ѷȣ�����