0.6
(1) K�ı���ʽΪ����?????????��??�������÷�Ӧ������ӦΪ����????????����Ӧ�������ȡ����ȡ���
(2) ���жϸ÷�Ӧ�Ƿ��Ѿ��ﵽ��ѧƽ��״̬���ǣ�???????????????
����������ѹǿ���䡡��??????�£����������COŨ�Ȳ���
�ã�v(H2)��= v(H2O)�桡��??? D��c(CO2) = c(CO)��
��3��ij�о�С�����÷�Ӧ��CO(g)+H2O(g)  ?H2(g)+CO2(g) ?��H=��41.2kJ/mol���Ʊ�CO2��H2�Ļ�����塣�ü�Һ����һ����CO2�ķ�������������H2��CO2������ȡ�����1L1.5mol/L��NaOH��Һ���������22.4L��������Ϊ��״���������CO2�������պ���Һ�и�����Ũ�ȴӴ�С��˳����????????????????????????????????�� ?H2(g)+CO2(g) ?��H=��41.2kJ/mol���Ʊ�CO2��H2�Ļ�����塣�ü�Һ����һ����CO2�ķ�������������H2��CO2������ȡ�����1L1.5mol/L��NaOH��Һ���������22.4L��������Ϊ��״���������CO2�������պ���Һ�и�����Ũ�ȴӴ�С��˳����????????????????????????????????��
��4���罫H2��CO2��4:1������Ȼ�ϣ����ʵ��������¿��Ƶ�CH4����֪��
CH4 (g) + 2O2(g)  ?CO2(g)+ 2H2O��1��??��H1����890.3 kJ/mol? ?CO2(g)+ 2H2O��1��??��H1����890.3 kJ/mol?
H2(g) + 1/2O2(g)  ?H2O��1��???????????��H2����285.8 kJ/mol? ?H2O��1��???????????��H2����285.8 kJ/mol?
��CO2(g)��H2(g)��Ӧ����CH4(g)��Һ̬ˮ���Ȼ�ѧ����ʽ��?????????????????????��
��5��������ȼ�ϵ������ͼ��
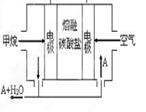
��ͼ��������̼����Ϊ����ʣ���CH4Ϊȼ�ϣ�����Ϊ��������ϡ����������Ϊ�缫����֪�����ĵ缫��Ӧ��CH4 +4CO32����8e��=5CO2+2H2O�������ĵ缫��Ӧ��_______?��Ϊ��ʹ��ȼ�ϵ�س�ʱ���ȶ����У���صĵ�������Ӧ�����ȶ���Ϊ�˵�ع���ʱ�����в���A���ʲμ�ѭ������A���ʵĻ�ѧʽ��_________��ʵ������У���ͨ���˱�״���¿���448L�����������O2�������Ϊ20%������������ȼ�ϵ�����ı�״����CH4____________L��
�ο��𰸣���1�� ��������� ���������
�����������1����ӦCO2(g) + H2(g)?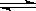 ??CO(g) + H2O(g) ƽ�ⳣ������ʽΪ ??CO(g) + H2O(g) ƽ�ⳣ������ʽΪ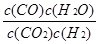 ���ɱ� ���ɱ�
�����Ѷȣ�һ��
2��ѡ���� ��֪25�棬Fe��OH��3��s�� Fe3+��aq��+3OH-��aq����Ksp��Fe3++3H2O Fe3+��aq��+3OH-��aq����Ksp��Fe3++3H2O Fe��OH��3+3H+��Kh��ˮ�����ӻ�����ΪKw������Ksp��Kh��Kw�Ĺ�ϵ�� Fe��OH��3+3H+��Kh��ˮ�����ӻ�����ΪKw������Ksp��Kh��Kw�Ĺ�ϵ��
A��Ksp��Kh=Kw3
B��Ksp��Kw=Kh
C��Kh/Kw=Ksp
D��Kw/Kh=Ksp3
�ο��𰸣�A
���������Ksp=c��Fe3+����c(OH-)3,Kh=c3(H+)/c(Fe3+)����Ksp��Kh=c3��H+����c3��OH-��=Kw3����ѡA��
�����Ѷȣ�һ��
3������� ��4�֣���֪������ˮ������ˮ�д����ܽ�ƽ�⣺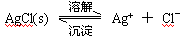
��һ���¶��£�ˮ��Һ��Ag+�����ʵ���Ũ�Ⱥ�Cl�������ʵ���Ũ�ȵij˻�Ϊһ���������� KSP��ʾ��KSP�� c(Ag+)��c(Cl-)��1.8��10-10��
��������AgCl�ֱ����� 100 mL����ˮ���� 100 mL 0.1 mol / L NaCl��Һ���� 100 mL 0.1 mol / L AlCl3��Һ���� 100 mL 0.1 mol / L MgCl2��Һ�У����������ͬ�¶���Ag+Ũ���ɴ�С��˳��(����Żش�)�� ______��______��______��______����0.1 mol / L AlCl3��Һ�У�Ag+�����ʵ���Ũ�����Ϊ_________mol / L��
�ο��𰸣�1? 2 ? 4 ?3��6�w 10-10
�����������
�����Ѷȣ�һ��
4��ѡ���� �����£�Ksp(CaSO4)=9��10-6��������CaSO4��ˮ�еij����ܽ�ƽ��������ͼ������˵����ȷ����

A�������£���100mL CaSO4������Һ�У�����400mL 0.01mol/LNa2SO4��Һ����Һ���г�������
B��b�㽫�г������ɣ�ƽ�����Һ��c(SO42-)һ������3��10-3 mol/L
C��d����Һͨ���������Ա䵽c��
D��a���Ӧ��Ksp����c���Ӧ��Ksp
�ο��𰸣�D
�����������Ŀ����ͼΪ��

A��������CaSO4������Һ�У�c��Ca2+��=c��SO42-��=3��l0-3mol/L������100mL CaSO4������Һ�У�����400mL 0.01mol/LNa2SO4��Һ����Һ�е�Qc=3��l0-3��1/5��0.01��4/5=4.8��l0-6<Ksp�������������
�����Ѷȣ���
5��ѡ���� ij�¶�ʱ��BaSO4��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵����ȷ����
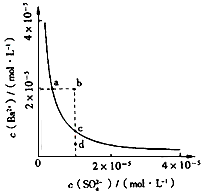
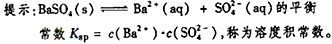 [???? ] [???? ]
A. ����Na2SO4����ʹ��Һ��a��䵽b��
B. ͨ����������ʹ��Һ��d��䵽c��
C. d����BaSO4��������
D. a���Ӧ��Ksp����c���Ӧ��Ksp
�ο��𰸣�C
���������
�����Ѷȣ�һ��
|