微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关概念的说法中正确的是
A.在101KPa下,1mol物质完全燃烧的反应热叫做该物质的热值
B.在化学反应中,能量较高、能发生碰撞的分子称为活化分子
C.具有相同质子数不同中子数的核素互称同素异形体
D.既可以与酸反应又可以与碱反应生成盐和水的氧化物称为两性氧化物
参考答案:D
本题解析:
试题分析:燃烧热是1mol可燃物完全燃烧生成稳定的氧化物所放出的热量,A错误;活化分子是能够发生有效碰撞的分子,B错误;质子数相同中子数不同的核素互称为同位素,C错误;能与酸和碱生成盐和水的氧化物是两性氧化物,D正确。
点评:理解概念中的关键词。
本题难度:一般
2、选择题 下列化学用语表达错误的是(???????? )
A.乙醇分子的比例模型图: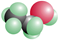
B.苯分子的最简式:CH
C.丙烯的结构简式:CH3CHCH2
D.甲基的电子式: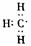
参考答案:C
本题解析:C、不符合C的四个价键的基本规则,烯烃要体现出碳碳双键;应为CH3CH=CH2。
本题难度:一般
3、填空题 (7分) 铜和浓硫酸发生反应的化学方程式为:
Cu +2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(1)浓H2SO4作_________剂,具有 性。
(2)在该反应中,若消耗了32 g Cu,则转移了___ ____mol 电子 ,还原了 mol H2SO4,生成 L SO2(标准状况)气体。
(3)以下三种物质的氧化性由强到弱的顺序为: (写出序号)
① 浓H2SO4 ②稀H2SO4 ③CuSO4
参考答案:(1)氧化,氧化, (2)1
本题解析:Cu +2H2SO4(浓) CuSO4+SO2↑+2H2O 转移电子物质的量
CuSO4+SO2↑+2H2O 转移电子物质的量
因为:64g 被还原硫酸1mol 22.4L(标况) 2mole-
所以:32g 被还原硫酸0.5mol 11.2L(标况) 1mole-
根据氧化剂的氧化性大于氧化产物:浓H2SO4氧化性大于CuSO4 ;随着反应的进行硫酸浓度逐渐变稀,硫酸的氧化性逐渐减弱,当变成稀硫酸反应就不能进行了,所以CuSO4的氧化性大于稀H2SO4。
本题难度:一般
4、计算题 (15分)用KMnO4氧化溶质质量分数为36.5%的盐酸。反应方程式如下:
2KMnO4+16HCl =2KCl+2MnCl 2+5Cl 2↑+8H2O
(1)若此盐酸的密度为1.2g/cm3,其物质的量浓度为
(2)用双线桥表示电子的得失
(3)此反应中氧化剂是 ,氧化产物
(4)若有x mol KMnO4参加反应,则转移电子的物质的量为
(5)15.8g KMnO4完全反应,产生标准状况下Cl2的体积为 ,同时有 mol HCl被氧化。
参考答案:(1)若此盐酸的密度为1.2g/cm3,其物质的量浓度为12
本题解析:
试题分析:(1)根据质量分数与物质的量浓度的换算公式得c=1000×密度×质量分数÷摩尔质量=1000×1.2×36.5%÷36.5=12mol/L。(2)在反应中锰元素化合价降低5价,得到的电子数为2×5,氯元素升高1价,失去的电子数为10×1,标出反应中的得失电子数。(3)反应中高锰酸钾中锰元素化合价降低,故为氧化剂,氯化氢中氯元素化合价升高到氯气,故氯气为氧化产物。(4)根据锰的化合价的变化可以知道,当有xmol KMnO4参加反应,则转移电子的数目为5x mol。(5)15.8g KMnO4为15.8÷158=0.1摩尔,根据反应方程式,完全反应产生Cl20.25摩尔,标准状况下体积为5.6L,同时有0.5 mol HCl被氧化。
考点:质量分数与物质的量浓度的换算,氯气的实验室制法,氧化还原反应中的转移电子数的计算。
本题难度:一般
5、选择题 向含有FeCl3、BaCl2的酸性溶液中通入SO2气体会有沉淀产生,该沉淀是
A.BaSO4
B.FeS
C.BaSO3
D.S
参考答案:A
本题解析:
试题分析:铁离子具有氧化性,能把SO2氧化生成硫酸,进而生成白色沉淀硫酸钡,答案选A。
点评:该题属于基础性试题,难度不大,关键是记住常见物质的化学性质。
本题难度:一般