微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是(??)

A.根据图①可判断可逆反应A2(g)+3B2(g) 2AB3(g)的ΔH>0
2AB3(g)的ΔH>0
B.图②表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
C.图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
D.根据图④,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量CuO,至pH约为4
参考答案:D
本题解析:
试题分析:A、根据图①可知,交点之前,反应未达平衡,交点时处于平衡状态,交点后增大温度逆反应速率增大比正反应速率增大更多,平衡向逆反应移动,升高温度平衡向吸热反应移动,故可判断可逆反应A2(g)+3B2(g)?2AB3(g)正反应是放热反应,故A错误;B、由图②可知,由甲到乙,到达平衡时间缩短,说明条件改变是乙的速率加快,平衡时反应物的转化率不变,改变条件变化不移动,对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,若乙的压强大,反应速率加快,但平衡向正反应移动,反应物的转化率增大,与
本题难度:一般
2、选择题 在25℃时建立下列平衡:2NO2?N2O4△H<0,若把烧瓶置于100℃的沸水中,下列情况:
①颜色?②平均摩尔质量?③质量?④压强?⑤密度,
其中达到新平衡前不变的是( )
A.③⑤
B.③④
C.②④
D.①③
参考答案:升高温度,化学平衡向着吸热方向进行,所以化学平衡2NO2?N
本题解析:
本题难度:简单
3、选择题 在一定温度下的密闭定容容器中,当下列叙述中的哪一项不再变化时,表明反应A(s)+2B(g)?C(g)+D(g)已达平衡( )
A.混合气体的压强
B.B的物质的量浓度
C.A的物质的量浓度
D.气体的总物质的量
参考答案:A、由于A是固体,反应方程式两边气体的化学计量数之和相等,气
本题解析:
本题难度:一般
4、选择题 已知NO2和N2O4可以相互转化:2NO2(g) N2O4(g)???△H <0。在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2 L的密闭容器中,反应物浓度随时间变化关系如图。下列说法不正确的是(?????)
N2O4(g)???△H <0。在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2 L的密闭容器中,反应物浓度随时间变化关系如图。下列说法不正确的是(?????)
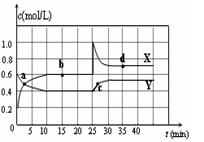
A.图中的两条曲线,X表示NO2浓度随时间的变化曲线
B.前10 min内用v(N2O4 ) =" 0.2" mol/(L・min)
C.25 min时,NO2转变为N2O4的反应速率增大,其原因是将密闭容器的体积缩小为1L
D.前10 min内用v(NO2) =" 0.04" mol/(L・min)
参考答案:BC
本题解析:
试题分析:由图中曲线变化的比例关系可知,△X:△Y=2:1,故X为N2O4浓度随时间的变化曲线,A项错误。v(NO2)= △c(NO2)/t="0.02" mol/(L・min),D项错误。
本题难度:一般
5、选择题 N2(g)+3H2(g) 2NH3(g) +92.4 kJ。恒容时,体系中各物质浓度随时间变化的曲线如图示。下列说法错误的是
2NH3(g) +92.4 kJ。恒容时,体系中各物质浓度随时间变化的曲线如图示。下列说法错误的是
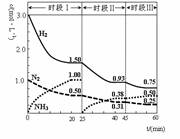
A.前20分钟反应内放出的热量为46.2kJ
B.第25分钟改变的条件是将NH3从反应体系中分离出去
C.若第60分钟时反应又达到了平衡,则时段Ⅲ改变的条件是增大压强
D.时段Ⅰ仅将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数不变
参考答案:AC
本题解析:
试题分析:A.由于不知道溶液的体积无法知道反应的量无法计算放出的热量,故A错误;B.第Ⅱ阶段氨气是从0开始的,瞬间A、B浓度不变,因此可以确定第一次平衡后从体系中移出了C,即减少生成物浓度,平衡正向移动,故B正确;C.第Ⅲ阶段的开始与第Ⅱ阶段的平衡各物质的量均相等,根据A、B的量减少,C的量增加可判断平衡是正向移动的,根据题目所给条件容器的体积不变,则改变压强也不可能,因此一定为温度的影响,此反应正向为放热反应,可以推测为降低温度,因此达到平衡后温度一定比第Ⅱ阶段平衡时的温度低,故C错误;D.D中
本题难度:一般