微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在一定温度下,下列叙述中属于可逆反应A(g)+B(g) 2C(g)达到平衡标志的是(???)
2C(g)达到平衡标志的是(???)
A.C的生成速率与C的分解速率相等
B.混合气体的压强不再变化
C.单位时间内消耗a mol A的同时消耗a mol B
D.A、B、C的物质的量之比为1∶1∶2
2、简答题 在一个2L的密闭容器中,发生反应2SO3(g)?2SO2(g)+O2(g);△H>0,其中SO3的变化如图所示:
(1)写出该反应的平衡常数表达式______.
(2)用O2表示0~8min内该反应的平均速率v=______.
(3)升高温度,该反应的反应速率将______;K值将______;容器中气体的平均相对分子质量将______.(填“增大”“减小”或“不变”)
(4)能说明该反应已达到平衡状态的是______
a.v(SO3)=2v(O2)??????????b.容器内压强保持不变?????? c.v逆(SO2)=2v正(O2)??????? ?d.容器内密度保持不变
(5)从8min起,压缩容器为1L,则SO3的变化曲线为______
A.?a??????B.?b??????C.?c???????D.?d.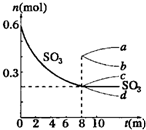
3、实验题 (7分)下表数据是在某高温下,金属镁和镍分别在氧气中进行氧化反应时,在金属表面生成氧化薄膜的实验记录。
反应时间t/h
| 1
| 4
| 9
| 16
| 25
|
MgO层厚y/nm
| 0.05a
| 0.20a
| 0.45a
| 0.18a
| 1.25a
|
NiO层厚y′/nm
| B
| 2b
| 3b
| 4b
| 5b
注:a和b均为与温度有关的常数。
(1)金属高温氧化腐蚀速率可以用金属氧化膜的生长速率来表示,其理由是_______________
_______________________________________________________________________________;
(2)金属氧化膜厚y跟时间t所呈现的关系是(填“直线”、“抛物线”、“对数”或“双曲线”等类型):MgO氧化膜的膜厚y与时间t的关系属________型;NiC氧化膜的膜厚y′与时间t的关系属________型;
(3)Mg与Ni比较,哪一种金属具有更良好的耐氧化腐蚀性?阐述其理由。
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
_______________________________________________________________________________。
4、选择题 在一定温度下,体积不变的密闭容器中可逆反应A(g)+3B(g)?2C(g)达到平衡的标志是( )
A.气体的密度不再变化
B.单位时间内生成n?molA,同时生成3n?molB
C.A、B、C的浓度不再变化
D.A、B、C的浓度之比为1:3:2
5、选择题 下列关于化学反应限度的说法正确的是( )
A.当一个可逆反应达到平衡状态时,这就是这个反应所能达到的限度
B.当一个可逆反应进行到平衡状态时,这个反应的正向反应速率和逆向反应速率相等
C.平衡状态是一种静止的状态,因为反应物和生成物的浓度已经不再改变
D.化学反应的限度不可以通过改变条件而改变
|