��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� .����ͬ�������кϳ�A(g)+2B(g) C(g)+2D(g)���ں��º��������·ֱ�����������ֲ�����
C(g)+2D(g)���ں��º��������·ֱ�����������ֲ�����
��������ʼ��1mol A��n molB
��������ʼ��1mol C��m molD
���ֲ���������ƽ���B�����������ͬ����A��B��ת������ͬ�������йص�˵����ȷ���ǣ�??��
A�����ֲ���������ƽ��������е�B��ת�������������C��ת����֮��Ϊ100%
B��n=1
C��m=1
D����A(g)+2B(g) C(g)+2D(g)���SH��0����t0ʱ�̴ﵽƽ�⣬����ѹǿ�������ʱ仯����ͼʾ���ɵ�ͼ
C(g)+2D(g)���SH��0����t0ʱ�̴ﵽƽ�⣬����ѹǿ�������ʱ仯����ͼʾ���ɵ�ͼ
�ο��𰸣�A
���������
���ֲ���������ƽ���B�����������ͬ����A��B��ת������ͬ��˵��Ͷ�ϱȷ��ϼ���ϵ���ȣ��Ҳ��������������ȫ��Ч������һ�ߵ���ת����A��C�����ʵ���Ϊ1mol������ȷ��n=2��m=2��ͼ��ĺ�����ʱ�䣬�����Ƿ�Ӧ���ʣ�t0ʱ�̴ﵽƽ�⣬�ı����������v��������v���棩��������v����������ķ��ȸ������ԣ�v��������v���棩��ƽ�������ƶ����˷�Ӧ������ӦΪ�����������ȵ����ȷ�Ӧ������ѹǿ����û��Ӱ�죬���������淴Ӧ���ʾ�����ƽ�������ƶ�����Ͷ�ϱȷ��ϼ���ϵ���ȣ����ֲ���������ƽ��������еķ�Ӧ���ת������������з�Ӧ���ת����֮��Ϊ100%��
�����Ѷȣ���
2������� CH3OH��g��+H2O��g��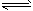 ?CO2��g��+3H2��g�����÷�Ӧ������ӦΪ���ȷ�Ӧ���������ĿҪ��ش��������⣺
?CO2��g��+3H2��g�����÷�Ӧ������ӦΪ���ȷ�Ӧ���������ĿҪ��ش��������⣺
��1���������������������½����¶ȣ����淴Ӧ����________�������С�����䡱����ͬ�����������������������¼�ѹ��������Ӧ����________��
��2��һ�������£������Ϊ2L���ܱ������г���1molCH3OH(g)��3molH2O(g)��20s��û�������ѹǿ�Ƿ�Ӧǰ��1��2�������ü״���ʾ�÷�Ӧ������Ϊ________________��
��3���жϸÿ��淴Ӧ�ﵽƽ��״̬�������ǣ�����ţ�________________����
A v����CH3OH��=v��(CO2)
B ���������ܶȲ���
C ��������ƽ����Է�����������
D CH3OH��H2O��CO2��H2��Ũ�ȶ����ٷ����仯
��4����һ�������£����÷�Ӧ���ڻ�ѧƽ��״̬ʱ�����в�����ʹ��ѧƽ�����淴Ӧ�����ƶ�����
________������ţ���
A�������¶ȡ�B�������¶ȡ�C������ѹǿ D����Сѹǿ��E�����������F���Ƴ�ˮ����
��5����ͼ��P�ǿ�����ƽ�л����Ļ������ر�K������ͬ�¶�ʱ����A�����г���1molCH3OH(g)��2mol
H2O(g)����B�����г���1��2molCH3OH(g) ��2��4molH2O(g)���������ֱ���������Ӧ����֪��ʼʱ����A��B�������ΪaL���Իش�
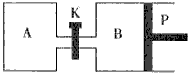
�ٷ�Ӧ�ﵽƽ��ʱ����B�����Ϊ1��5aL������B��CH3OHת����Ϊ________��A��B��������H2O��g��������ٷֺ����Ĵ�С��ϵΪ��B________���>������<������=���� A��
������K��һ��ʱ������´ﵽƽ�⣬����B�����Ϊ________L����ͨ��������������Բ��ƣ��Ҳ������¶ȵ�Ӱ�죩��
�ο��𰸣���1����С������
��2��0.01mol/��L��s��<
���������
�����Ѷȣ�����
3��ѡ���� ��BaO2�����ܱյ���������У���Ӧ2BaO2(s) 2BaO(s)+O2(g)�ﵽƽ�⡣�����¶Ȳ��䣬��С�����ݻ�����ϵ���´ﵽƽ�⣬����˵����ȷ����
2BaO(s)+O2(g)�ﵽƽ�⡣�����¶Ȳ��䣬��С�����ݻ�����ϵ���´ﵽƽ�⣬����˵����ȷ����
A��ƽ�ⳣ����С
B��BaO������
C������ѹǿ����
D��BaO2������
�ο��𰸣�CD
���������
���������A.ƽ�ⳣ��ֻ���¶��йأ��¶Ȳ��䣬ƽ�ⳣ���Ͳ��䡣����B. �÷�Ӧ������Ӧ�������������ķ�Ӧ�������¶Ȳ��䣬��С�����ݻ���Ҳ��������ѹǿ������ƽ���ƶ�ԭ������ѧƽ�������������С�ķ�Ӧ�������淴Ӧ�����ƶ�������BaO����С������C�������¶Ȳ��䣬��ѧƽ�ⳣ���Ͳ��䣬����ֵ�͵���������Ũ�ȣ�Ũ�Ȳ��䣬���ѹǿ���䡣��ȷ��D. ��С�����ݻ���ƽ�������ƶ���������ϵ���´ﵽƽ��BaO2�����ӡ���ȷ��
�����Ѷȣ�һ��
4������� ��10�֣����淴Ӧ2SO2 + O2  2SO3���е�ʱ��(t)�ͷ�Ӧ�������SO3�İٷֺ����Ĺ�ϵ��ͼ��ʾ����ش��������⣺
2SO3���е�ʱ��(t)�ͷ�Ӧ�������SO3�İٷֺ����Ĺ�ϵ��ͼ��ʾ����ش��������⣺
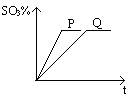
��1�������������Ϊ����������ͬ���ֱ�Ϊʹ�úͲ�ʹ�ô�����������?????��ʾʹ���˴��������Ҵ�ͼ���֪����������??????????????????????????????????????������????????????????????????
��2�����������������÷�Ӧ��Ӧ���ʵ�������ʩ?????????????��???????????????��
�ο��𰸣���10�֣���1��P������Ӧ���ʣ������ܸı䷴Ӧ���е���<
�����������
�����Ѷȣ���
5��ѡ���� ���й������ʡ���Ӧ�̶ȡ���˵����ȷ���ǣ�??��
A��һ�������£�2molsO2������O2��Ӧ�ɵõ�2molsO3
B����4mol HCl��Ũ������������MnO2���ȷ�Ӧ���Ʊ�1mol Cl2
C��10mL 18.0mol/L H2SO4������ͭ���ȷ�Ӧ���Ʊ�0.09molsO2
D��һ�������£�1mol N2��3mol H2��Ӧ���Ʊ�1.0mol NH3
�ο��𰸣�D
�����������ΪSO2��O2�ķ�Ӧ��N2��H2�ķ�Ӧ���ǿ��淴Ӧ����Ӧ�ﲻ������ȫת��Ϊ�������A����ȷ��D��ȷ��MnO2ֻ����Ũ���ᷴӦ��ȡCl2����4mol HCl��Ũ����������MnO2��Ӧ������Cl2������1mol��BҲ����ȷ��
�����Ѷȣ�һ��