微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、推断题 镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、炭粉、氧化铁等涂覆在铝箔上制成.由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行资源回收研究,并设计出相关实验流程图
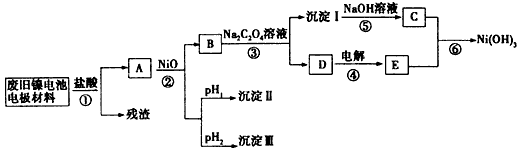
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+
②某温度下一些金属氢氧化物的Ksp及沉淀析出的理论pH如表所示:

回答下列问题:
(1)根据表数据判断步骤②依次析出沉淀Ⅱ 和沉淀Ⅲ (填化学式),则pH1 pH2(填填“>”、“=”或“<”),控制两种沉淀析出可利用 。
A.pH试纸 B.石蕊指示剂 C.pH计
(2)已知溶解度:NiC2O4>NiC2O4?H2O>NiC2O4?2H2O,则反应③的化学方程式是 。第③步反应后,过滤沉淀时需要的玻璃仪器有 。若过滤时发现滤液中有少量浑浊,从实验操作的角度给出两种可能的原因 、 。
(3)④中阳极反应产生的气体E为 ,验证该气体的试剂为 。
(4)试写出反应⑥的离子方程式 。
参考答案:(1)Fe(OH)3 A
本题解析:由题给条件,金属氢氧化物的Ksp及沉淀析出的理论pH,可知,在A溶液中加入NiO是为了调节溶液pH,使相应的铝离子、三价铁离子全部沉淀出,Ni2+在溶液B中.根据pH可以确定开始析出沉淀和全部沉淀的pH范围,先析出沉淀Ⅱ是Fe(OH)3,沉淀pH范围是2.53~2.94,然后析出沉淀Ⅲ是Al(OH)3,沉淀PH的范围3.43~4.19,所以pH1<pH2;控制两种沉淀析出必须准确测定pH值,所以应利用pH计测定。
(2)由溶解度:NiC2O4>NiC2O4?H2O>NiC2O4?2H2O,结合流程中的变化
可知沉淀为溶解度小的NiC2O4?2H2O,所以根据转化关系写出化学方程式;
在过滤装置中用到的玻璃仪器和注意问题,根据装置和操作步骤写出NiCl2+Na2C2O4+2H2O=NiC2O4・2H2O+2NaCl,漏斗,烧杯、玻璃棒;滤纸破损、过滤液的液面高于滤纸的边缘。
(3)由流程图和以上分析可知,D溶液主要是氯化钠溶液,电解氯化钠溶液在阳极得到氯气,阴极得到氢气,所以E气体是Clc 2,验证氯气的试剂应是淀粉碘化钾溶液,遇氯气变蓝;
(4)在B溶液中加入Na2C2O4溶液生成了沉淀ⅠNiC2O4.2H2O,沉淀中加入氢氧化钠溶液,根据Ni(OH)2开始沉淀到全部沉淀的pH范围为7.60~9.75,加入过量氢氧化钠溶液能使沉淀NiC2O4・2H2O转化为Ni(OH)2,所以C为沉淀Ni(OH)2;根据流程图中的转化关系,沉淀C和氯气能生成Ni(OH)3,镍元素化合价升高是被氯气氧化的结果,因此离子方程式为2Ni(OH)2+2OH-+Cl2=2Ni(OH)3+2Cl-
本题难度:困难
2、选择题 按图甲装置进行实验,实验结果如图乙所示.乙中横坐标x表示电路中通过电子的物质的量,纵坐标y表示反应物或生成物的物质的量,下列叙述不正确的是( )
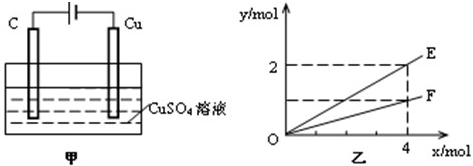
A.E表示反应生成铜的物质的量
B.E表示反应消耗水的物质的量
C.F表示反应生成氧气的物质的量
D.F表示反应生成硫酸的物质的量
参考答案:由甲可知,为电解装置,C为阳极,发生4OH--4e-=O2↑
本题解析:
本题难度:一般
3、选择题 化学兴趣小组的同学用如图实验装置电解硫酸铜溶液,a、b为惰性电极。则下列说法错误的是
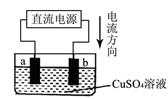
A.a是电解池的阴极、b是电解池的阳极
B.b电极上的电极反应为:4OH--4e-=2H2O + O2↑
C.通电一段时间后,溶液的PH减小
D.通电一段时间后,欲使电解液恢复到起始状态,应向溶液中加入适量的CuSO4
参考答案:D
本题解析:
试题分析:由图可知,电流由正极流向负极,则b为阳极,a为阴极,故A正确;则b为阳极,发生氧化反应,4OH--4e-= 2H2O + O2↑,故B正确;根据电解总反应2CuSO4+2H2O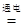 2Cu+O2↑+2H2SO4,所以溶液PH减小,故C正确;根据电解总反应,欲使电解液恢复到起始状态,应向溶液中加入适量的CuO,故D错误
2Cu+O2↑+2H2SO4,所以溶液PH减小,故C正确;根据电解总反应,欲使电解液恢复到起始状态,应向溶液中加入适量的CuO,故D错误
考点:本题考查电解原理。
本题难度:一般
4、选择题 下列关于电解的说法正确的是
A.工业上通常用电解饱和食盐水生产金属钠,电解熔融氯化铝冶炼铝
B.电镀时,通常把待镀的金属制品做阳极
C.电解法精炼铜时,其含有的Zn、Fe、Ni、Ag、Au等杂质沉积在电解槽的底部
D.二次电池充电过程的实质是电解,充电时应将其负极与充电器电源的负极相连
参考答案:D
本题解析:钠和铝属于活泼的金属,其阳离子在水溶液中不能放电。电解饱和食盐水生成物是氯气、氢气和氢氧化钠,电解熔融的氯化钠才能生成钠。氯化铝不是离子化合物,熔融状态不能导电,冶炼铝电解的是熔融的氧化铝,A不正确。电镀时,通常把待镀的金属制品做阴极,镀层金属作阳极,含有镀层金属离子的溶液作电镀液,B不正确。银和金的活泼性弱于铜的,在粗铜精炼时,银和金不能失去电子,而是形成了阳极泥。但Zn、Fe、Ni等金属活泼性强于铜,可以失去电子被溶解,C不正确。充电电池负极发电时发生氧化反应,所以充电时就要发生还原反应,由此和电源的
本题难度:一般
5、填空题 (14分)能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应I:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
反应II:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
上述反应符合“原子经济”原则的是 (填“I”或“Ⅱ”)。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1275.6 kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH=-566.0 kJ/mol
③H2O(g)=H2O(l) ΔH=-44.0 kJ/mol
则CH3OH(l)+O2(g)=CO(g)+2H2O(l) ΔH=
(3)某实验小组依据甲醇燃烧的反应原理,设计如下图所示的电池装置。
①该电池负极的电极反应为 。
②工作一段时间后,测得溶液的pH (填增大、不变、减小)。
③用该电池作电源,组成如下图所示装置(a、b、c、d均为石墨电极),甲容器装250mL0.04mol/LCuSO4溶液,乙容器装300mL饱和NaCl溶液,写出c电极的电极反应 ,常温下,当300mL乙溶液的pH为13时,断开电源,则在甲醇电池中消耗O2的体积为 mL(标准状况),电解后向甲中加入适量下列某一种物质,可以使溶液恢复到原来状态,该物质是 (填写编号) 。

A.CuO
B.CuCO3
C.Cu(OH)2
D.Cu2(OH)2CO3
参考答案:(1)I (2分) (2)ΔH=
本题解析:
本题难度:困难