微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用NaCl固体配制0.1 mol・L-1的NaCl溶液,下列操作或说法正确的是(???)
A.将5.85gNaCl固体溶于1 L水中可配成0.1 mol・L-1的NaCl溶液
B.定容时仰视观察液面,实验结果偏低
C.固体溶解后,将溶液转移到容量瓶中,然后向容量瓶中直接加水稀释到刻度线
D.配制溶液时容量瓶中原来有少量蒸馏水不会影响实验结果
参考答案:BD
本题解析:
试题分析:A项:1 L水的体积并不是溶液的体积,溶液体积大于水的体积,配制溶液的溶度会小,故错;C项:将溶液转移到容量瓶中,要左右震荡容量瓶,故错。故选BD。
点评:本题考查的是溶液的配制。学生要掌握住其步骤,才能正确的解答此类问题。
(1)计算:计算配制所需固体溶质的质量或液体浓溶液的体积。
(2)称量:用托盘天平称量固体质量或用量筒(应用移液管,但中学阶段一般用量筒)量取液体体积。
(3)溶解:在烧杯中溶解或稀释溶质,恢复至室温(如不能完全溶解可适当加热)。检查容量瓶是否漏水
(4)转移:将烧杯内冷却后的溶液沿玻璃棒小心转入一定体积的容量瓶中(玻璃棒下端应靠在容量瓶刻度线以下)。
(5)洗涤:用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液转入容器中,振荡,使溶液混合均匀。
(6)定容:向容量瓶中加水至刻度线以下1cm~2cm处时,改用胶头滴管加水,使溶液凹面恰好与刻度线相切。
(7)摇匀:盖好瓶塞,用食指顶住瓶塞,另一只手的手指托住瓶底,反复上下颠倒,使溶液混合均匀。
最后将配制好的溶液倒入试剂瓶中,贴好标签。
影响:
1.称量时引起误差。
2.未将烧杯洗涤,使溶液的物质量减少,导致溶液浓度降低。
3.转移时不小心溅出溶液,导致浓度偏低。
安全注意:
1.氢氧化钠为碱性化学物质,浓盐酸为酸性化学物质,注意不要溅到手上、身上、以免腐蚀!
2.要注意计算的准确性
3.注意移液管的使用
4.稀释浓硫酸是把酸加入水中,用玻璃棒搅拌。
5.容量瓶在使用前必须检漏,检漏的步骤为注入自来水至标线附近,盖好瓶塞.右手托住瓶底,倒立2min,观察瓶塞是否渗水。如不漏,将塞子旋转180度,再检漏.如漏水,需换一套容量瓶,再检漏。
6.在配置由浓液体稀释而来的溶液时,如由浓硫酸配置稀硫酸时,不应该洗涤用来称量浓硫酸的量筒,因为量筒在设计的时候已经考虑到了有剩余液体的现象,以免造成溶液物质的量的大小发生变化!
7.移液前应静置至溶液温度恢复到室温(如氢氧化钠固体溶于水放热,浓硫酸稀释放热,硝酸铵固体溶于水吸热),以免造成容量瓶的热胀冷缩!
本题难度:简单
2、填空题 (1)用18mol・L-1的硫酸配制1.00 mol・ 的硫酸100mL。若实验仪器有:
的硫酸100mL。若实验仪器有:
A.100mL量筒、B.托盘天平、C.玻璃棒、D.50mL容器瓶、E. 10mL量筒、
F.胶头滴管、G. 50mL烧杯、H. 100mL容量瓶。
实验时应选用仪器是??????????????????????????????(填 字母);
字母);
(2)在容量瓶的使用方法 中,下列操作不正确的是??????????????(填字母);
中,下列操作不正确的是??????????????(填字母);
A.使 用容量瓶前检查其是否漏水。
用容量瓶前检查其是否漏水。
B.容量瓶用蒸馏水洗净后,再用待配溶液洗涤。
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近刻度线1―2cm处,用胶头滴管滴加蒸馏水到刻度线。
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近刻度线1―2cm处,用胶头滴管滴加蒸馏水到刻度线。
E.盖好瓶盖,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇动多次
(3)浓H2SO4稀释时应该??????????????????????????????????????????????????????????
???????????????????????????????????????????????????????????????????????????????;
(4)若实验遇到下列情况,对硫酸溶液的物质的量浓度有何影响?(填“偏高”、“偏低”或“不变”)
①稀释硫酸后的烧杯未洗涤:????????????;
②未经冷却趁热将溶液注入容量瓶中:????????????;
③摇匀后发现液面低于刻度线再加水:????????????;
④容量瓶中原有少量蒸馏水:?????????????。
参考答案:实验时应选用仪器是? CEFGH???????????
本题解析:略
本题难度:简单
3、选择题 根据下列实验现象,所得结论正确的是(???)
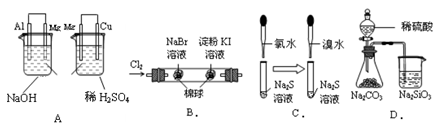
实验
| 实验现象
| 结论
|
A.
| 左烧杯中镁表面有气泡,右边烧杯中铜表面有气泡
| 活动性:Al>Mg>Cu
|
B.
| 左边棉花变为橙色,右边棉花变为蓝色
| 氧化性:Cl2>Br2>I2
|
C.
| 左边溶液产生黄色沉淀,右边溶液产生黄色沉淀
| 氧化性:Cl2>Br2>S
|
D.
| 锥形瓶中有气体产生,烧杯中液体变浑浊
| 非金属性:S>C>Si
?
参考答案:D
本题解析:A选项结论不正确;金属活动性仍然是:Mg>Al>Cu。虽然在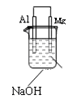 该原电池中镁表面有气泡属于原电池的正极,AL属于负极,但活动性还是Mg>Al,造成这种现象的原因是,只有AL才能与NaOH溶液反应,而镁不能与NaOH溶液反应。所以,一般,我们在判断原电池的正、负时不能一概而论地说活性强的金属一定是属于原电池的负极,还要结合电解质溶液。 该原电池中镁表面有气泡属于原电池的正极,AL属于负极,但活动性还是Mg>Al,造成这种现象的原因是,只有AL才能与NaOH溶液反应,而镁不能与NaOH溶液反应。所以,一般,我们在判断原电池的正、负时不能一概而论地说活性强的金属一定是属于原电池的负极,还要结合电解质溶液。
B选项左边棉花变为橙色是发生了反应:CL2 + 2NaBr == 2NaCL + Br2;说明氧化性:Cl2>Br2。右边棉花变为蓝色可能发生的反应:CL2 + 2KI== 2KCL + I2:也可能发生的反应:Br2 + 2KI== 2KBr + I2:不能得出Br2>I2的结论。
C选项只能得出氧化性:Cl2>S:Br2>S而得不到氧化性:Cl2>Br2
D选项正确;锥形瓶中有气体产生,烧杯中液体变浑浊说明:酸性:H2SO4>H2CO3>H2SiO3;对于非金属元素来说,最高价氧化物对应的水化物―酸性越强则非金属越强。
本题难度:简单
4、选择题 某学习小组拟利用如下装置制备氮化钙(化学式:Ca3N2, 极易与H2O反应),下列说法正确的是
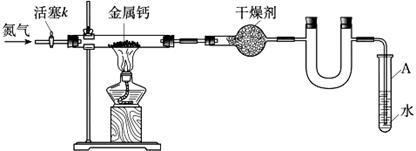
A.打开活塞K通入N2,试管A内有气泡产生,说明装置气密性良好
B.U形管中盛放的干燥剂既可以用碱 石灰,也可以用浓硫酸 石灰,也可以用浓硫酸
C.反应结束后,先熄灭酒精灯,待反应管冷却后再关闭活塞K
D.将产物Ca3N2放入盐酸中,只能得到一种盐
参考答案:C
本题解析:略
本题难度:一般
5、选择题 可用下图所示装置制取(必要时可加热)、净化、收集的气体是???
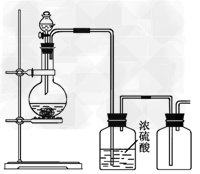 [???? ] [???? ]
A.铜与稀硝酸反应制一氧化氮
B.氯化铵与氢氧化钙固体反应制氨气
C.锌和稀硫酸反应制氢气
D.亚硫酸钠固体与浓硫酸反应制二氧化硫
参考答案:D
本题解析:
本题难度:一般
|