��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
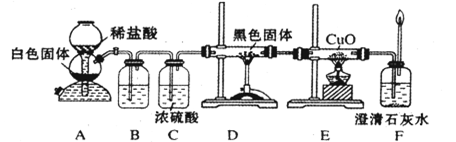
1��ʵ���� �������֣�CO���л�ԭ�ԣ�ij��ѧ�о�С��Ϊ֤��CO���л�ԭ�ԣ��������ͼ��ʾ��ʵ��װ�á�
��֪��C + H2O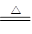 CO+H2?? CO + H2O
CO+H2?? CO + H2O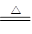 ?CO2 + H2?? C + CO2
?CO2 + H2?? C + CO2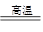 2CO
2CO
�Իش���������:
��װ��B�������˵��Լ���???????????????��������װ��C���������е�ˮ������������????????????????????????????????????????????????��
�ڸ��ݸ�ʵ���е�?????????????????????????????����֤��CO���л�ԭ�ԣ�
����Ҫ����װ��F��ʯ��ˮ����ǵ�����ȷȷ��CO���л�ԭ�ԣ���Ӧ����ͼװ��????��?????֮��(����ĸ���)������ͼ�е�??????????װ��(ѡ�����)��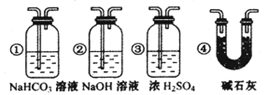
�ο��𰸣��ٱ���NaHCO3��Һ��2�֣�?��ֹˮ������̿��Ӧ���ɵ�����
�����������1������A������CO2�к����Ȼ��⣬����B�������dz�ȥ�Ȼ��⣬�ñ���̼��������Һ���Ȼ��⡣�����ڸ����£�ˮ�����ܺ�̼��Ӧ����������CO������Ũ����������Ƿ�ֹˮ������̿��Ӧ���ɵ�������ʵ������������š�
��2��CO��ԭ����ͭ������CO2��ͭ��������� Eװ���к�ɫCuO��ɺ�ɫ��˵��CO���л�ԭ�ԡ�
��3������CO2��̼��Ӧʱ��CO2��������ȫ�����գ�����Ҫ����װ��F��ʯ��ˮ����ǵ�����ȷȷ��CO���л�ԭ�ԣ���Ӧ�ó�ȥ�����CO2������Ӧ����ͼװ��D��E֮�����Ӣܡ�
�����Ѷȣ�һ��
2��ѡ���� ����װ�ÿ�������ʵ������ȡ��Ȳ����ķ�Ӧװ�õ���
A��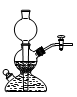
B��
C��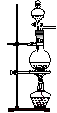
D��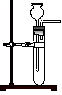
�ο��𰸣�B
���������ʵ��������̼������ʳ��ˮ�����·�Ӧ��ȡ��Ȳ���壬���þƾ��Ƽ��ȣ��ų�C����Ϊ�÷�Ӧ���ң����ȶ࣬�������ɵ��������Ƴʺ�״���������շ������������װ�õ��¶˹ܿڣ����ų�A��D��
��ѡB
�����Ѷȣ�һ��
3��ʵ���� ��12�֣����������(NH4)2SO4?FeSO4?6H2O��һ����Ҫ��ѧ�Լ���ʵ�����ó�ȥп�Ʋ����Ƭ����ȡ��������泥��������£�
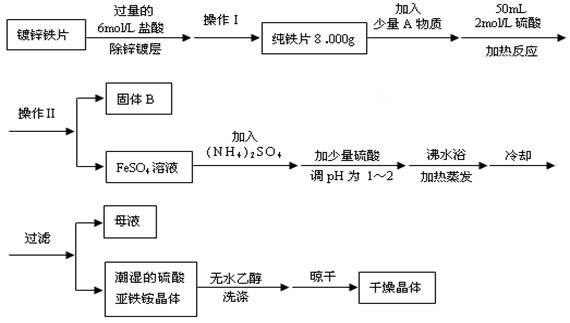
��ش��������⣺
��1��ȷ��п�Ʋ㱻��ȥ�ı�־��?????????????????????????��
����������Ƭп�Ʋ�ĺ�ȣ�����Ҫ��������????????????�����ţ���
a��п���ܶȦѣ�g/cm3��????? b����п��Ƭ����m 1��g��?? c������Ƭ����m 2��g��
d����п��Ƭ���S��cm2��??? e����п��Ƭ���h��cm��
��2�����������У���������ȡ����Ƭ��???????��????????��������
��3��A���ʿ���Ϊ????????�����ţ���
a��CuCl2?????? b��CuO?????? c��Cu(NO3)2?????? d��CuSO4??
��4������ˮ�Ҵ�ϴ�ӳ�ʪ����������茶�����Ϊ�˳�ȥ������������ˮ�֣����ü��Ⱥ�ɵ�ԭ����???????????????????��
��5���������þ����к���Fe2����NH4����SO42�����ӵ�ʵ�鷽����ȷ����?????�����ţ���
a��ȡ������Ʒ���Թܣ���ˮ�ܽ⣬ͨ������Cl2���ټ�KSCN��Һ���۲�����
b��ȡ������Ʒ���Թܣ���ˮ�ܽ⣬����NaOH��Һ��¶���ڿ����У��۲�����
c��ȡ������Ʒ���Թܣ���ˮ�ܽ⣬����ŨNaOH��Һ�����ȣ���ʪ��ĺ�ɫʯ����ֽ�����Թܿڣ��۲���ֽ��ɫ�ı仯
d��ȡ������Ʒ���Թܣ���ˮ�ܽ⣬����������ټ���BaCl2��Һ���۲�����
�ο��𰸣���12�֣���1����Ӧ����ͻȻ��С������Ƭ�������ɵ�����ͻȻ��
�����������1�������������û�����������п�Ľ������Խ���ǿ���ʵ���Ƭ�������ɵ�����ͻȻ����ʱ������п�Ʋ��ѱ���ȥ
п�������Ϊ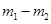 �������Ϊ
�������Ϊ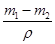 ������п��Ϊ���棬��п����Ϊ
������п��Ϊ���棬��п����Ϊ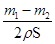 ���ʼ���п�Ʋ�ĺ�Ȳ���Ҫ����п��Ƭ��ȡ�
���ʼ���п�Ʋ�ĺ�Ȳ���Ҫ����п��Ƭ��ȡ�
��2������I��Ϊ�����ʵ�龫�ȣ����뽫��Ƭ����ϴ�Ӹɾ����ٸ�������
��3������ԭ��ط�Ӧ���ʿ��ڻ�ѧ��Ӧ��ͬʱΪ���������ʣ��ʿ�ͨ������CuO��CuSO4�γ���ͭԭ��أ��Լӿ췴Ӧ����
B�����ǹ����������û���ͭ
��4�����ڲ�Ʒ�ֽⲢ���ױ��������ʾ���������
��5��a����ʹ������Fe2+������Ҳ�ɳ���Ѫ��ɫ������ȷ
b��ͨ�����ɰ�ɫ������������ɫ�ı仯���ɼ����Fe2+�Ĵ��ڣ���ȷ
c:�����ݳ�����ֽ��ɫ��������ȷ
d�����Լ����SO42�D���ӵĴ��ڣ���ȷ
�����Ѷȣ�һ��
4��ʵ���� ʵ������ͨ����MnO2��Ũ���ᷴӦ��ȡ�������䷴Ӧ�Ļ�ѧ����ʽΪ��
MnO2��4HCl��Ũ��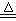 Cl2����MnCl2��2H2O
Cl2����MnCl2��2H2O
�Իش��������⣺
��1���÷�Ӧ��������ԭ��Ӧ�𣿢�???????����ǡ����ǡ����������������ԭ��Ӧ��ָ������������???????????���ۻ�ԭ����?????????????����д���÷�Ӧ������ ����ʽ?????????????????????????????????????????????????????????????��
����ʽ?????????????????????????????????????????????????????????????��
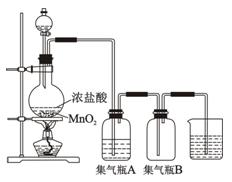
��2������ƿA��ʢװ���DZ���ʳ��ˮ��ע�������ڱ���ʳ��ˮ���ܽ�Ⱥ�С������
�����ڱ���ʳ��ˮ�е��ܽ����ܴ���������????????????????????????????��
��3����������ˮ�����ԣ��������ж������о��ҵĴ̼��ԣ��������������������
����������������β��ֱ����������У�����Ⱦ������ʵ�����пɲ���???????????��Һ�������ж���������
��4��һ��ʵ���У�����Ũ����200mL�����ܶ�Ϊ1.19g��cm-3��HCl����������Ϊ36.5%��
��MnO2�պ���ȫ��Ӧʱ��������5.6L����״������������
�Լ����Ũ��������ʵ���Ũ�Ⱥͱ�������HCl�����ʵ���������д��������̣�
�ο��𰸣���1���� �ǣ��� MnO2���� Ũ���
�� 4H
�����������
�����Ѷȣ���
5��ʵ���� ����װ��Ϊ��ѧ��ѧʵ�鳣�õ������Ʊ�װ��
 ???????
??????? ??????
??????
A???????????? B????????? C
��1������NaHCO3��ϡ������ȡ������̼��Ӧѡ��װ�� ???????????��
��2������NH4Cl�ͼ�ʯ����ȡNH3��Ӧѡ��װ�� ????????????????��
��3�����ø�����غ�Ũ���������ȡCl2��Ӧѡ��װ��???????????��
��4����ij�о���С��������ϵ�֪��Ư����������Һ��Ӧ���Ƶ���������ѧ����ʽΪ��Ca(ClO)2+CaCl2+2H2SO4="2" CaSO4+2 Cl2+2H2OӦѡ��װ��?????????��
��Ϊ֤���������������Խ������ֱ�ͨ�뵽����������Һ���Ȼ�������Һ�У����ʵ��֤�����������Ѿ������� ?????????????????????????????????????????????????????????????��
д���������Ȼ�������Һ��Ӧ�����ӷ���ʽ��???????????????????????????????????��
����д������β�����������ӷ���ʽ ????????????????????????????????????????????��
�ο��𰸣���1��A��2��C��3��A ��4���� A ��ȡϴ��ƿ��C�е���
���������
�����������1������NaHCO3��ϡ������ȡ������̼��Ӧѡ��װ���ǹ����Һ��֮�䲻��Ҫ���ȵģ���˷�����������װ��A��
��2������NH4Cl�ͼ�ʯ����ȡNH3��Ӧѡ��װ���ǹ��������Ҫ���ȵģ���˷�����������ѡ��C��
��3�����ø�����غ�Ũ���������ȡCl2��Ӧѡ��װ���ǹ����Һ��֮�䲻��Ҫ���ȵģ���˷�����������װ��A��
��4���ٸ��ݷ�Ӧ�ķ���ʽ��֪Ca(ClO)2+CaCl2+2H2SO4��2CaSO4+2Cl2+2H2O���÷�Ӧ�ǹ����Һ��֮�䲻��Ҫ�����Ʊ�����ģ�����Ӧ��ѡ��װ��A��
�����������ᱵ������ˮ����������ˮ���С������ᱵ������ˮ��Ҳ�������ᣬ����֤�����������Ѿ�������ʵ�鷽����ȡϴ��ƿ��C�е���Һ����������BaCl2��Һ���ټ���ϡ���ᣬ��������ɫ��������֤��Na2SO3�ѱ��������������Ȼ�������Һ��Ӧ�����ӷ���ʽ��Fe2++ Cl2��2 Fe3++2 Cl-��
�������ж�����Ҫβ��������һ��������������Һ���գ���Ӧ�����ӷ���ʽ��Cl2+2OH-��Cl-+ClO-+ 2H2O��
������������Ҫ�ǿ���ѧ������װ�õ�ѡȡ������Ӧ�ü�����ʽ����д��֪ʶ�����ԺܺõĿ���ѧ������֪ʶ�������Ӧ������������������ѧ���������������淶�Ͻ���ʵ���������������������ѧ����ѧ�����������ѧ����Ӧ��������ѧϰЧ�ʡ�
�����Ѷȣ�һ��