��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �Ȼ���(BN)������һ���������ϳɲ��ϡ�����ɰ(Na2B4O7)�����ط�Ӧ���Եõ�������Na2B4O7+ 2CO(NH2)2��4BN+Na2O +4H2O+2CO2��������Ҫ��ش��������⣺
��1����ɷ�Ӧ�������Ԫ���У���һ������������___________________��
��2�����ط���( )��
)��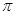 ����
����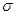 ����Ŀ֮��Ϊ__________�����ط����д���ͬһƽ���ԭ�������_______����
����Ŀ֮��Ϊ__________�����ط����д���ͬһƽ���ԭ�������_______����
��3�����ط���һ���������γ������Ρ������ӡ����ṹ��ͼ�����������ӡ������ط��Ӽ���Ҫͨ��ʲô��������ϡ���________________(��1��)��

��4��ͼʾ�������ӡ������᷽����һ��ͨ������ֱ���������Ӹպ��ܽ���ͨ�������γɡ������ӡ��İ�̨�֧���������в������ռ�����ϴ�������롰ͨ������������һ���ʿ���ʵ��ֱ��������֧�������ķ��롣
��ֱ�����������ܽ���ͨ��ʱ��ͨ��ʲô�������롰�����ӡ���ϣ��Ӷ��γ� �������ӡ�������?��___________________��
���������ʿ���ͨ�����ء������ӡ����з������____________��
A������Ͷ���??? B��������춡��??? C���������������??? D�Ȼ��ƺ��Ȼ���
��5��BN������a��B�������ͣ���a��BN�ṹ��ʯī���ơ�B��BN�ṹ����ʯ���ơ�
��aһBN������Nԭ���ӻ���ʽ��____________________��
��B��BN�����У�ÿ����ԭ���γ�________�����ۼ�����Щ���ۼ��У���________��Ϊ��λ����
�ο��𰸣���1��N��2�֣�
��2��1�U7��2�֣�?? 6��2�֣�
���������
�����������1����ɷ�Ӧ�������Ԫ��Na��B��O��C��N��H���ǽ�����Խǿ��һ������Խ�����ڵ�Ԫ�ص�2p������Ӵ��ڰ����״̬���ȶ���ǿ�����Ե�Ԫ�صĵ�һ�����ܴ�����Ԫ�صģ�����ɷ�Ӧ�������Ԫ���У���һ������������N��
��2����������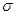 ����˫������1��
����˫������1�� �����Ѷȣ�һ��
�����Ѷȣ�һ��
2��ѡ���� ������������δ�ɼ��ŶԵ��ӵ���[???? ]
A��OH-
B��NH3
C��CH4
D��HCl
�ο��𰸣�C
���������
�����Ѷȣ���
3������� һˮ�����İ���ͭ(��)([Cu(NH3)4]SO4��H2O)��һ����Ҫ��Ⱦ�ϼ�ũҩ�м��塣��ش������������:
(1)Cu�ĺ�������Ų�ʽΪ???????��
(2)N��L������???????�ԳɶԵ���;N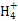 ���幹����???????,������ԭ�ӵ��ӻ���ʽΪ???????��
���幹����???????,������ԭ�ӵ��ӻ���ʽΪ???????��
(3)��ˮ��Һ�д��ڶ������,�α�ʾ����������???????;
(4)[Cu(NH3)4]SO4��H2O�г�����ɫ��������???????,�����еġ����ӶԸ���һ���ܼ�������???????��;
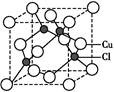
(5)Cu��һ���Ȼ��ᄃ���ṹ��ͼ��ʾ,���Ȼ���Ļ�ѧʽ?????��
�ο��𰸣�(1)1s22s22p63s23p63d104s1
(
���������(1)Cu�ڵ�4���ڢ�B��,�����Ų�Ϊ1s22s22p63s23p63d104s1;(2)N�ĵ����Ų�ʽΪ1s22s22p3,L���Ӳ㼴�ڶ��ܲ�,���ֻ��1�ԳɶԵ���,N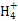 ����ԭ�ӵ�ԭ�Ӳ���sp3�ӻ�,�ռ乹��Ϊ����������;(3)��ˮ��Һ�а������ӺͰ�������֮������γ����,ˮ���Ӻ�ˮ����֮������γ����,ˮ����
����ԭ�ӵ�ԭ�Ӳ���sp3�ӻ�,�ռ乹��Ϊ����������;(3)��ˮ��Һ�а������ӺͰ�������֮������γ����,ˮ���Ӻ�ˮ����֮������γ����,ˮ����
�����Ѷȣ�һ��
4��ѡ���� ����˵����ȷ����
A����Щ�������ɷ���ֱ�ӹ��ɵģ���ѧʽ��ȷ��ʾ�����ʷ�����ɣ�����ף�P4����������̼��CO2�����Ȼ�泥�NH4Cl����
B��C2H2��BeCl2�����е�����ԭ���ӻ������������ͬ
C����1molSiO2����������2molSi-O��
D�����ױ��ķе�˳���ǣ��ڶ��ױ�>�Զ��ױ������ǻ�����ȩ�ķе�˳���ǣ����ǻ�����ȩ >���ǻ�����ȩ
�ο��𰸣�B
���������
���������A��Ȼ�泥�NH4Cl�������ӻ��������������ɵģ��ʴ���C�1 mol SiO2�к���4 mol Si��O�����ʴ���D����ǻ�����ȩ�ķе�������ǻ�����ȩ��ԭ���ǣ����ǻ�����ȩ���ڷ����������ʹ�۷е㽵��(��ʵ�ǡ�ռ�ݷ��Ӽ������λ�á�)�����ǻ�����ȩ���ڷ��Ӽ������ʹ�۷е����ߣ����ǻ�����ȩ�ķе�˳���ǣ����ǻ�����ȩ <���ǻ�����ȩ���ʴ�����ѡB��
���������⿼����ǻ�ѧʽ��ԭ���ӻ������ԭ�Ӿ��塢��������֪ʶ����Ŀ�Ѷ��еȣ�ע��һЩ�����Ϲ��ɵ��������ʡ�
�����Ѷȣ�һ��
5��ѡ���� ����˵������ȷ���� [???? ]
A�����й��ۼ��Ļ�����һ���ǹ��ۻ����� ����
B���ڹ��ۻ�������һ�����й��ۼ�
C���������Ӽ��Ļ�����һ�������ӻ����� ����
D��˫ԭ�ӵ��ʷ����еĹ��۽�һ���ǷǼ��Լ�
�ο��𰸣�A
���������
�����Ѷȣ���