微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列离子方程式不正确的是
A.碳酸氢钙溶液跟盐酸反应:Ca(HC03)2+2H+=Ca2++2H20+2C02↑
B.碘化钾溶液跟适量溴水反应:2I一+Br2=I2+2Br―
C.将金属锂加入水中:2Li+2H20=2Li++20H一+H2↑
D.将氯气通人氯化亚铁溶液中2Fe2++C12=2Fe3++2Cl一
参考答案:A
本题解析:
试题分析:A、碳酸氢钙属于易溶易电离的盐,书写离子方程式时应拆开,错误;B、溴单质氧化碘离子为碘单质,符合离子反应方程式的书写原则,正确;C、锂与水反应生成氢氧化锂和氢气,符合离子方程式的书写原则,正确;D、氯气氧化亚铁离子为铁离子,正确,答案选A。
本题难度:一般
2、填空题 某溶液甲中可能含有下列离子中的几种:K+、NO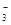 、SO
、SO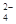 、NH
、NH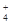 、CO
、CO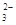 (不考虑溶液中由水电离的少量的H+和OH-),取200mL该溶液,分为两等份进行下列实验:
(不考虑溶液中由水电离的少量的H+和OH-),取200mL该溶液,分为两等份进行下列实验:
实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为672mL;
实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33g。
(1)甲溶液中一定存在的离子是??????????????????;
(2)甲溶液中一定不存在的 离子是?????????????????;
(3)甲溶液中可能存在的离子是??????????????????????;你得出此结论的理由是????????????????????????????????????????????????。
参考答案:(1)NO 本题解析:
本题解析:
试题分析:(1)根据实验1:第一份加入足量的烧碱并加热,因NH4++OH-=NH3↑+H2O,会产生标准状况下为224mL气体,证明含有NH4+,且物质的量为0.01mol;
实验2:第二份先加入足量的盐酸,无现象,则一定不含有CO32-,再加足量的BaCl2溶液,得固体2.33g,证明一定含有SO42-,且物质的量为:n="m/M" ="2.33g/233g/mol" =0.01mol;根据溶液中的电荷守恒,溶液呈电中性,则一定含有钾离子,且钾离子的浓度≥0.01mol×2?0.01mol
本题难度:一般
3、填空题 (4分)在水溶液中,短周期元素Y形成的YO3n-与S2-能发生如下离子反应:
YO3n-+3S2-+6H+???Y-+3S↓+3H2O???请回答:
(1)此反应中,氧化剂是_____________。??????(2)YO3n-中n= _______。
(3)Y元素在周期表中位于????周期?????族。
参考答案:(4分) (1)YO3n-?? (2) 1?? (3)???
本题解析:略
本题难度:简单
4、选择题 向Ba(OH)2溶液中逐滴滴入稀硫酸,下列溶液的导电能力描述正确的是(??? )
A.开始时导电能力肯定最强
B.当沉淀为最大值时,导电性最弱
C.先变强,后变弱
D.逐渐变弱
参考答案:B
本题解析:向Ba(OH)2溶液中逐滴滴入稀硫酸,则溶液的导电能力应该是先变弱,再增强,如果硫酸的浓度大于Ba(OH)2溶液的浓度,最终溶液中离子的浓度可能比开始时的浓度大,所以A、C、D错误;当二者恰好完全反应时,此时沉淀量达到最大值,溶液呈中性,溶液离子浓度最小,导电性最弱,B正确。
本题难度:简单
5、选择题 某溶液中,滴加KSCN溶液时无明显现象发生,再滴入少量氯水,溶液立即显红色。则原溶液里一定含有的是?????
A.Fe2+
B.Fe3+
C.Al3+
D.NH4+
参考答案:A
本题解析:
试题分析:溶液中加入KSCN溶液无明显现象,说明溶液中无Fe3+;再加少量氯水,溶液变红,说明加入氯水生成了Fe3+,原溶液中存在Fe2+。
点评:检验Fe3+常用KSCN溶液;检验Fe2+时,先加KSCN溶液,无现象,再加少量氯水或双氧水,溶液呈红色。
本题难度:简单