��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ͼװ��(��)Ϊһ�ֿɳ���ص�ʾ��ͼ,���е����ӽ���Ĥֻ����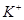 ͨ�����õ�طŵ�ʱ�Ļ�ѧ����ʽΪ:
ͨ�����õ�طŵ�ʱ�Ļ�ѧ����ʽΪ: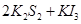 ?��
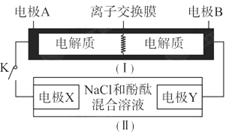
?��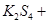 3KI��װ��(��)Ϊ���ʾ��ͼ�����պϿ���Kʱ���缫X������Һ�ȱ�졣��պ�Kʱ,����˵����ȷ����?(??? )
3KI��װ��(��)Ϊ���ʾ��ͼ�����պϿ���Kʱ���缫X������Һ�ȱ�졣��պ�Kʱ,����˵����ȷ����?(??? )
 ?
?
A��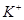 ���ҵ���ͨ�����ӽ���Ĥ
���ҵ���ͨ�����ӽ���Ĥ
B���缫A�Ϸ����ķ�ӦΪ: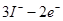 ��
��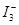
C���缫X�Ϸ����ķ�ӦΪ: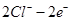 ��
��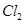 ��
��
D������0.1 mol 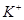 ͨ�����ӽ���Ĥ��X�缫�ϲ���1.12 L����(��״��)
ͨ�����ӽ���Ĥ��X�缫�ϲ���1.12 L����(��״��)
�ο��𰸣�D
������������պϿ���Kʱ���缫X������Һ�ȱ�죬ʯīX�缫�������������ӷŵ磬�ƻ�ˮ�ĵ���ƽ�⣬�Ӷ�����OH�����缫A�Ǹ�����B��������ѡ��C����ȷ��ԭ������������������ƶ�������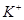 ������ͨ�����ӽ���Ĥ��A����ȷ������ʧȥ���ӣ������ܵķ�Ӧʽ��֪������X��S22��ʧȥ���ӣ�B����ȷ�����ݵ��ӵĶ����غ��֪��ͨ��0.1mo
������ͨ�����ӽ���Ĥ��A����ȷ������ʧȥ���ӣ������ܵķ�Ӧʽ��֪������X��S22��ʧȥ���ӣ�B����ȷ�����ݵ��ӵĶ����غ��֪��ͨ��0.1mo
�����Ѷȣ�һ��
2������� ��12�֣��о������ĸ�ʴ��������зdz���Ҫ�����塣
��1�����ĵ绯ѧ��ʴ�������֣������ָ�ʴ�ĸ�����Ӧ��Ϊ??????????????????????����������Ӧ���������ˮĤ����Ծ�������ˮĤ��Ƚϸ�ʱ��������ӦʽΪ????????????????????????�����ָ�ʴ��Ϊ???????��ʴ����ˮĤ���Բ�ǿʱ��������ӦʽΪ??????????????????????????�����ָ�ʴ��Ϊ??????��ʴ��
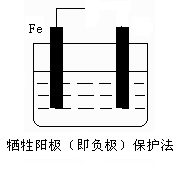
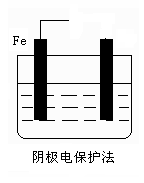
��2����ֹ������ʴ�ĵ绯ѧ���������֣���ͼ��Һ��Ϊ��ˮ������ͼ�����ӱ�Ҫ�ĵ��ߡ���Դ��ע����һ�缫�ĵ缫�������ƣ�ʹ�����ͼ����ע�ı���������
 ??
??
�ο��𰸣���1�����缫��Ӧʽÿ��2�֣�����ÿ��1�֣�
Fe -2
�����������������ĸ�ʴ�����
��1�����������绯ѧ��ʴ����������ʧȥ���ӣ�����������Ӧʽ��Fe -2e�C =Fe2+ ����ˮĤ��Ƚϸ�ʱ���������ⸯʴ��������ӦʽΪ2H++ 2e�C = H2������ˮĤ���Բ�ǿʱ������������ʴ��������ӦʽΪO2+2H2O+ 4e�C =4OH�C��
��2���绯ѧ��ֹ������ʴ�ķ��������֣��ֱ���������������������������ӵ����������������������ͼ����Ҫһ�ֽ�����ǿ�����ģ�����п������ͼ����Ӧ�����������͵�Դ�ĸ���������������ȷ��ͼʾ�� �����Ѷȣ�һ��
�����Ѷȣ�һ��
3��ѡ���� ������ѧϰ��������������۲������������绯��ʴ�йص���
A�����������г���Ȧ��������
B�������˵�����δ��ʱϴ�����ֺ��ɫ���
C��������ͭ˿�ڻ��������պ���
D��ʵ����þ��������һ��ʱ�������Ұ�
�ο��𰸣�B
������������г���Ȧ���ںϽ𣬲������⣻ͭ����ʱ���������ɺ�ɫ����ͭ��þ�ǻ��õĽ��������ױ���������Щ������绯ѧ��ʴ��ϵ�ġ�ѡ��B���Ǹ����ĵ绯ѧ��ʴ�����Դ�ѡB��
�����Ѷȣ���
4������� ��8�֣�����š��ɴ��ķ���ɹ�����־���ҹ�������ҵ����������ҵ��
��1��.ȼ�ϵ�صķ�չ�ͺ���������ܲ��ɷ֡�ȼ�ϵ�ز�������ת���ʸߣ�����������������Ϊȼ�ϵĵ�أ���ط�Ӧ���ɵ�ˮ���ɹ��Ա���á�
��ʹ�����Ե���ʵ�����ȼ�ϵ�أ������ĵ缫��ӦΪ????????????????????????????��
�������İ������·ɴ�ʹ�õ��Ǽ�������ȼ�ϵ�أ������ĵ缫��ӦΪ
O2 + 2H2O + 4e�� = 4OH���������ĵ缫��ӦΪ?????????????????????????????��
����ͼ������̼����ȼ�ϵ�صĹ���ԭ��ʾ��ͼ��

��֪�����ĵ缫��ӦΪ2 H?2 �C 4e��+ 2CO32�� ="2" H2O +2CO2��
�����ĵ缫��ӦΪ??????????????????????????????????????????????????��
��2��.̫���ܵ��ҲΪ����ɴ��ṩ�˷������Դ���ں���ɴ���H2O��O2��ѭ���У�����̫���ܵ�أ�����ͨ�����ˮ�ṩO2������4 mol���ӷ���ת�ƣ����������ϵõ�������������״������?????????L��
�ο��𰸣���1���� H2 �� 2e- =? 2H+??�� H2 �� 2
���������
�����������1������ȼ�ϵ���У������������Խ���ʱ��������ӦΪH2-2e- = 2H+��������ӦΪO2+4H++4e-=2H2O���������Ǽ��Խ���ʱ��������ӦΪH2-2e-+ 2OH- = 2H2O��������ӦΪO2 + 2H2O+4e��= 4OH����������ȼ�ϵ��������ӦʽΪO2+4e-=2O2-��O2-+CO2=CO32-����ʽ�ϲ���O2+4e-+2CO2=2CO32-�������ܷ�Ӧʽ2H2+O2=2H2O��ȥ������Ӧʽ��������ӦʽO2+4e-+2CO2=2CO32-��
��2�����ˮ��������
�����Ѷȣ�һ��
5��ѡ���� ����������ڳ��ͷŵ�ʱ�����ķ�Ӧ��Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2�����жԸ������ƶϴ�����ǣ�
Fe(OH)2+Ni(OH)2�����жԸ������ƶϴ�����ǣ�
�� �ŵ�ʱ��Fe���븺����Ӧ��NiO2����������Ӧ
�� ���ʱ�������ϵĵ缫��ӦʽΪ��Fe(OH)2+2e����Fe+2OH��
�� �ŵ�ʱ���������Һ�е��������������ƶ�
�� �ŵ�ʱ�������ϵĵ缫��ӦʽΪ��Fe+2H2O��2e����Fe(OH)2+2H+
�� ���صĵ缫�������ij�ּ��Ե������Һ��
A����
B���ۢ�
C����
D���٢ڢ�
�ο��𰸣�C
���������
����������ٷŵ���ԭ��أ��ɵ���ܷ�Ӧʽ��֪�ŵ�ʱFeԪ�صĻ��ϼ����ߣ���������ӦΪԭ��صĸ�����NiO2����������Ӧ���ʢ���ȷ���ڳ���ǵ��أ��ɷ���ʽ��֪�˵��Ϊ���Ե�أ���Ӧ����ʽʱ���ܳ���H+�����Գ��ʱ�����������ĵ缫��Ӧʽ�ͷֱ�Ϊ��Fe(OH)2+2e-��Fe+2OH-��2Ni(OH)2��2OH--2e-��Ni2O3��3H2O���ʢ���ȷ���۷ŵ�ʱ��ԭ��أ�������Fe-2e-+2OH-��Fe(OH)2��������NiO2+2e-+2H2O��Ni(OH)2+2OH-���������Һ�е���������
�����Ѷȣ�һ��