实验现象
A
取第一份溶液,向其中滴加几滴酚酞试液,反复振荡.
溶液不变红色
B
取第二份溶液,先加水稀释,再加少量的二氧化锰,有气泡放出,反复振荡,过滤,向滤液中滴加几滴酚酞试液,反复振荡.
溶液变红色
C
取第三份溶液,向其中先加少量的二氧化锰,有气泡放出,反复振荡,过滤,向滤液中滴加几滴酚酞试液,反复振荡.
溶液也不变红色
D
取第四份溶液,先加水稀释,再滴加几滴酚酞试液,反复振荡.
溶液也不变红色
试回答:
(1)按要求写出下列反应的化学方程式:
①过氧化钠与水反应生成过氧化氢和氢氧化钠:______.
②在二氧化锰作用下过氧化氢发生分解反应:______.
(2)根据B、D两个实验,回答D实验中酚酞试液不变红的原因是______.
(3)综合考虑,回答A实验中酚酞试液不变红的原因可能是:①______;②______.
参考答案:(1)①过氧化钠和水反应生成过氧化氢和氢氧化钠,反应方程式为
本题解析:
本题难度:一般
2、选择题 将标准状况下2.24LCO2缓慢通入100mL1.5mol・L-1NaOH溶液中(溶液体积变化忽略不计),充分反应后,下列关系正确的是(??? )
A.c( )>c( )>c( ) )
B.c( )+c( )+c( )="1" mol・L-1 )="1" mol・L-1
C.c(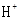 )>c( )>c(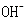 ) )
D.c(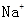 )+c( )+c(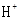 )=c( )=c( )+2c( )+2c( )+c( )+c(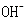 ) )
参考答案:D
本题解析:CO2的物质的量是0.1mol,而氢氧化钠的物质的量是0.15mol,所以在反应中生成的碳酸钠和碳酸氢钠分别都是0.05mol。由于碳酸钠的水解程度大于碳酸氢钠的水解程度,因此 c( )<c( )<c( 本题难度:一般 本题难度:一般
3、选择题 暴露在空气中不易变质的是? (????? )?
A.氯水
B.钠
C.氢氧化钠
D.氯化钠
参考答案:D
本题解析:氯水不稳定,长时间放置将变为盐酸。钠被氧化,氢氧化钠易吸水和二氧化碳,生成碳酸钠,所以正确的答案是D。
本题难度:简单
4、判断题 用金属钠制取氧化钠通常采用下法:2NaNO2+6Na=4Na2O+N2↑,试说明为什么用此法制取氧化钠比直接钠氧化法好。
参考答案:Na2O在N2气中不被氧化,从而分析出Na直接氧化法不足之处
本题解析:这题属于信息给予题,解答中必须紧扣题干Na2O制取反应式:2NaNO2+6Na=4Na2O+N2↑,反应中生成N2这一重要信息,才可找出答案:Na2O在N2气中不被氧化,从而分析出Na直接氧化法不足之处;无论金属钠是在氧气中点燃,还是在空气中氧化,因生成的Na2O极不稳定,会进一步氧化生成Na2O2,即2Na+O2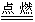 本题难度:简单 本题难度:简单
5、选择题 2003年诺贝尔化学奖授予美国科学家Peter Agre和Roderick Mackinnon以表彰他们在“水通道”和“离子通道”的研究成果。Mackinnon教授的研究内容主要是Na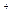 、K 、K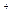 虽然体积很接近,但在生物体内呈现的差别却高达1万倍,他让科学家们观测到Na 虽然体积很接近,但在生物体内呈现的差别却高达1万倍,他让科学家们观测到Na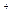 、K 、K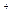 在进入离子通道前、通道中以及穿过通道后的状态,在医学应用上可为病人在“离子通道”中寻找具体的病因,并研制相应药物。下列关于钠、钾的说法正确的是(?) 在进入离子通道前、通道中以及穿过通道后的状态,在医学应用上可为病人在“离子通道”中寻找具体的病因,并研制相应药物。下列关于钠、钾的说法正确的是(?)
A.质钠的密度比钾的密度小
B.和钾在空气中燃烧的产物都是过氧化物
C.一小块钠投入盛5 mL澄清石灰水的试管里,可能观察到溶液变浑浊
D.和钾的合金〔w(K)=50%~80%〕熔点比钠和钾都高
参考答案:C
本题解析:本题以诺贝尔化学奖获得者的研究成果为背景命题,考查了金属钠、钾的性质和用途(新考纲增加知识点)及溶解度变化等知识点。详细的解答过程为:碱金属的密度总体上随原子序数增大而增大,但钠的密度反常(比钾大);钠在空气中燃烧的产物是过氧化钠,但钾在空气中燃烧的产物中还有超氧化钾;将钠投入澄清石灰水中会和水发生反应且放出热量,若石灰水是饱和的(氢氧化钙的溶解度随温度升高而减小),则会有少量Ca(OH)2析出来。
本题难度:简单
|