微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述中正确的是(??)
A.1 mol氢的质量是1 g
B.1 mol CO的质量为28 g・mol-1
C.阿伏加德罗常数等于6.02×1023
D.3.01×1023个SO2分子约是0.5 mol
参考答案:D
本题解析:
试题分析:A中1 mol氢指代不明,无法计算; B、1 mol CO的质量为28 g;C、阿伏加德罗常数约等于6.02×1023个; D、3.01×1023个SO2分子约是0.5 mol正确。
本题难度:一般
2、选择题 在t℃时,将a?gNH3完全溶解于水,得V?mL饱和溶液,测得该溶液的密度为ρg/cm3,质量分数为ω,其中n(NH4+)?为b?mol.则下列叙述中错误的是( )
A.溶液中C(OH-)=
1000b+C(H+)V
V
mol/L
B.溶质的物质的量浓度C=1000a
17V
mol/L
C.溶质的质量分数:ω=a
ρV+a
×100%
D.上述溶液中再加入VmL水后,所得溶液的质量分数小于0.5ω
参考答案:A、V?mL饱和溶液中n(OH-)=n(H+)+n(NH4+
本题解析:
本题难度:一般
3、选择题 用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B.25℃,1.01×105Pa,32gO2和O3的混合气体所含原子数为2NA
C.在常温常压下,44gCO2含有的原子数为3NA
D.标准状况下,11.2LH2O 含有的分子数为0.5NA
参考答案:BC
本题解析:
试题分析:A、氦气为单原子分子,一个原子就组成一个分子,故含有NA个氦原子的氦气的物质的量为1mol,在标准状况下的体积约为22.4L,错误;B、O2和O3都由O构成,而O的摩尔质量为16g/mol,故32g O2和O3的混合气体所含原子的物质的量为2mol,原子数为2NA,正确;C、在常温常压下,44gCO2的物质的量为1mol,一个含有CO2含有3个原子,故所含原子数为3NA,正确;D、标准状况下,H2O为液体或固体,错误;故选BC。
考点:考查阿伏伽德罗常数的应用。
本题难度:一般
4、选择题 用NA表示阿伏加德罗常数的值,下列说法中不正确的是
A.1L 0.01mol/L的氯水中含有的分子总数大大超过0.01 NA
B.92gNO2和N2O4混合气体中含有的氧原子总数为4NA
C.含NA个氧原子的O2与含NA个氧原子的O3的分子个数之比为3:2
D.5.6g Fe 与足量的Cl2充分反应,转移的电子 数目为0.2NA
参考答案:D
本题解析:
试题分析:A.由于氯水中存在水分子故含有的分子总数大大超过0.01 NA,正确。B. 92gNO2和N2O4最简式相同,质量相同时氧原子总数必相同为4NA,正确。C. 含NA个氧原子的O2与含NA个氧原子的O3的分子个数之比为3:2,正确。D.5.6g Fe 与足量的Cl2充分反应,转移的电子数目正确为0.3NA,故错误。
本题难度:一般
5、选择题 在VL硫酸铝溶液中,含有Wg?Al3+,则溶液中SO42-物质的量浓度为
A.W/27V
B.W/54V
C.W/18V
D.W/9V
参考答案:C
本题解析:分析:根据n= 计算Al3+的物质的量,根据电荷守恒3n(Al3+)=2n(SO42-),据此计算n(SO42-),再根据c= 计算Al3+的物质的量,根据电荷守恒3n(Al3+)=2n(SO42-),据此计算n(SO42-),再根据c=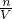 计算SO42-的浓度. 计算SO42-的浓度.
解答:Wg?Al3+的物质的量为 = =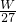 mol, mol,
根据电荷守恒3n(Al3+)=2n(SO42-),所以n(SO42-)= n(Al3+)= n(Al3+)= × ×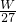 mol= mol=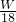 mol, mol,
故溶液中SO42-的浓度为: = =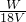 mol/L, mol/L,
故选C.
点评:本题考查物质的量浓度的有关计算,难度不大,计算硫酸根的物质的量是关键,注意对物质的量浓度定义式的理解.
本题难度:一般
|
|
|
网站客服QQ: 960335752 - 14613519 - 791315772