微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 酸奶中含有乳酸,其结构简式为
CH3―CH(OH)―COOH。
(1)乳酸跟足量金属钠反应的化学方程式为:_______________________________________。
(2)乳酸跟少量碳酸钠溶液反应的化学方程式为:_________________________________。
(3)乳酸在浓硫酸的存在下,3分子相互反应,生成物为链状,其结构简式可表示为:
______________________________________________________________________________。
(4)乳酸在浓硫酸存在下,2分子相互反应,生成物为环状,其结构简式为:
______________________________________________________________________________。
参考答案:(1)CH3―CH(OH)―COOH+2Na![]()
本题解析:(1)―OH和―COOH与钠均能发生反应,据此可写出反应的化学方程式。
(2)―COOH与Na2CO3反应放出CO2,而―OH与Na2CO3不反应,据此可写出反应的化学方程式。
(3)3分子乳酸在浓硫酸存在下,一分子中的―COOH与另一分子中的―OH酯化,相互作用可生成链状酯。
(4)2分子乳酸在浓硫酸存在下,2分子中的―OH和―COOH相互酯化,可生成环状交酯。
本题难度:简单
2、选择题 乙酸分子中的O都是18O,乙醇分子中的O都是16O,二者在一定条件下反应所得生成物中水的相对分子质量是(?? )
A.16
B.18
C.20
D.22
参考答案:C
本题解析:根据酯化反应的断键规律,该反应的化学方程式为:
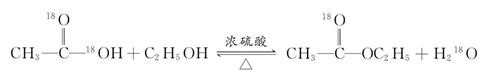
故C选项正确。
本题难度:一般
3、选择题 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法不正确的是
 [???? ]
[???? ]
A. 该硫酸的物质的量浓度为18.4 mol/L
B. 配制500 mL 3. 68 mol/L的稀硫酸,需取该硫酸100.?0 mL
C. 该硫酸与等体积的水混合,所得溶液的质量分数大于49%
D. 该硫酸50 mL与足量的铜充分反应,可得到标准状况下SO2 20.6L
参考答案:D
本题解析:
本题难度:简单
4、简答题 某化学课外兴趣小组为探究铜与浓硫酸的反应,用右图所示的装置进行实验:
请回答下列问题:
(1)B是用来收集实验中产生气体的装置,但未将导管画全,请将装置图补充完整.
(2)实验中他们取6.4g铜片和12mL18mol?L-1浓硫酸放在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有铜片剩余,该小组中的同学认为还有一定量的硫酸剩余.
①写出铜与浓硫酸反应的化学方程式:______,
实验中若有mg铜参加了反应,则有______mol硫酸被______(填“氧化”或“还原”),转移电子的物质的量为______mol.
②下列试剂中,能证明反应停止后烧瓶中有硫酸剩余的是______(填写字母编号).
A.硫酸钠溶液B.氯化钡溶液C.银粉D.碳酸钠溶液
③为什么有一定量的硫酸剩余但未能使铜片完全溶解?你认为的原因是______
(3)为了测定剩余硫酸的物质的量浓度,该兴趣小组设计了三个实验方案:
方案一:将装置A产生的气体缓缓通过已称量过的装有碱石灰的干燥管,反应停止后再次称量,两次质量差即是吸收的二氧化硫.
方案二:将装置A产生的气体缓缓通入足量的用硫酸酸化的高锰酸钾溶液,再加入足量的氯化钡溶液,过滤、洗涤、干燥,称得沉淀的质量即是二氧化硫转化为硫酸钡沉淀的质量.
方案三:当铜和浓硫酸的反应结束后,在装置A中加入足量的锌粉,用排水法测得产生氢气的体积为VL(已换算为标准状况).
实际上,以上方案一、二均不可取,请你说出原因?
方案一______;
方案二______.
方案三:写出剩余硫酸的物来源:91 考试网质的量浓度的计算式(假设反应后溶液的体积仍为12mL)______.
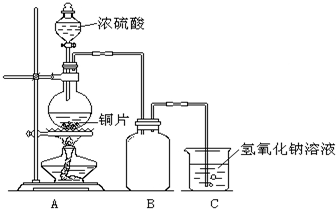
参考答案:(1)铜和浓硫酸加热一生成二氧化硫气体,二氧化硫比空气重,用
本题解析:
本题难度:简单
5、简答题 硫酸是一种实验室常用的化学试剂.请按要求填空:
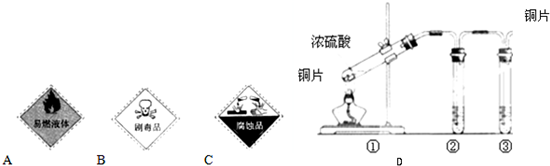
(1)浓硫酸试剂瓶上适合贴上的图标是______(填写字母标号).
(2)实验室有1.00mol?L-1的硫酸溶液,从中准确量出10.00mL,其物质的量浓度为______mol?L-1.现将准确量出的10.00mL的硫酸溶液配制成0.100mol?L-1的稀硫酸,所需要的玻璃仪器除烧杯、玻璃棒还需______和______.
(3)用图D所示的实验装置验证铜与浓硫酸反应生成的气体产物,则装置②、③试剂依次为下列的______和______
A.品红溶液B.BaCl2溶液 C.NaOH溶液D.AgNO3溶液
(4)装置①中发生反应的化学方程式为______,若装置①中加入铜6.4g和含有0.2molH2SO4的浓硫酸,则产生二氧化硫质量______
A.等于6.4克B.大于6.4克C.小于6.4克D.不能确定
(5)若将装置①中的铜片换成木炭,装置②试管内为品红溶液,装置③试管内为澄清石灰水,则装置①中发生反应的化学方程式为______.装置②中的现象是______.根据装置③观察到有白色沉淀生成的现象,______(填“能”或“不能”)判断该白色沉淀一定只有CaCO3.
参考答案:(1)浓硫酸具有腐蚀性,适合贴上的图标是图中的C,故答案为:
本题解析:
本题难度:简单