微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 由锌、铁、铝、镁四种金属的两种组成的混合物10克,与足量的盐酸反应产生的氢气在标准状况下的体积为11.2升,则混合物中一定含有的金属是
A.锌
B.铁
C.铝
D.镁
参考答案:C
本题解析:
试题分析:n(H2)=0.5mol,生成H2时得到1mol电子,若全由Zn提供则需32.5g,Fe则28g,Al则9g,Mg则12g,两种金属组成的混合物其平均值为10g,则必有金属铝。故选C。
本题难度:一般
2、选择题 设NA为阿伏加德罗常数的数值,下列说法正确的是
A.常温下,23g NO2含有NA个氧原子
B.1 L 0.1 mol?L-1的氨水含有0.1NA个OH
参考答案:
本题解析:
本题难度:一般
3、选择题 只给出下列甲中和乙中对应的量,不能组成一个求物质的量的公式的是
| ①
| ②
| ③
| ④
| ⑤
|
甲
| 物质粒子数
| 标准状况下气体摩尔体积
| 固体体积
| 溶质的质量分数
| 非标准状况下物质的质量
|
乙
| 阿伏加德罗常数
| 标准状况下气体体积
| 固体密度
| 溶液的体积
| 物质的摩尔质量
A.②③④ B.③④⑤ C.③④ D.③
参考答案:C
本题解析:由n=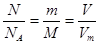 可知①②⑤正确。对③而言由固体体积和密度可求出固体的质量而不知摩尔质量,故无法求出n;对于④,n=cV(aq)= 可知①②⑤正确。对③而言由固体体积和密度可求出固体的质量而不知摩尔质量,故无法求出n;对于④,n=cV(aq)=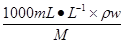 ×V(aq),因缺少溶液的密度和溶质的摩尔质量,无法求出n。 ×V(aq),因缺少溶液的密度和溶质的摩尔质量,无法求出n。
本题难度:一般
4、选择题 向27.2Cu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO 和Cu(NO3)2。在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g。下列有关说法正确的是
A.Cu与Cu2O 的物质的量之比为1:1
B.硝酸的物质的量浓度为2.6mol/L
C.产生的NO的体积为4.48L
D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol
参考答案:D
本题解析:39.2g沉淀是氢氧化铜,物质的量是0.4mol。如果设铜和氧化亚铜的物质的量分别是x和y,则64x+144y=27.2g和x+2y=0.4mol,解得x=0.2mol,y=0.1mol,所以选项A不正确;反应中共转移电子是0.2mol×2+0.1mol×2=0.6mol,所以根据电子的得失守恒可知,生成NO是0.6mol÷3=0.2mol,但体积不一定是4.48L,选项C不正确;生成物硝酸钠是1mol,所以原硝酸的物质的量是1mol+0.2mol=1.2mol,浓度是1.2mol÷0.5L=2.4mol/L,选项B不正确;生成硝酸铜是0.4mol,所以剩余硝酸是1.2mol-0.4mol×2-0.2mol=0.2mol,选项D正确,答案选D。
本题难度:一般
5、选择题 下列说法正确的是
A.2mol的盐酸
B.0.1mol氢
C.0.3molHCl
D.4mol的氧元素
参考答案:C
本题解析:用摩尔表示物质的量的单位时必须要用化学式指明粒子的种类,否则造成表达不清楚,所以
A错,盐酸为混合物,是物质不是微观粒子;B错,0.1mol氢指代不明,是氢离子还是氢原子或氢分子;C正确;D错,通常用化学式指明,不是元素符号;
本题难度:简单
|