微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 设NA表示阿伏加德罗常数的值,下列叙述中正确的是:
A.含4.8g 碳元素的石墨晶体中的共价键数是0.8NA
B.标准状况下,11.2LCO和N2的混合气体中,含有的原子数为NA
C.1mol的羟基(-OH)与1mol的氢氧根离子(OH-)所含电子数均为9NA
D.常压、500℃、催化条件下,1molSO2和0.5molO2充入一密闭容器内,充分反应后的生成物分子数为NA
参考答案:B
本题解析:
试题分析:A、石墨晶体中,每个C原子与其他C原子形成3个共价键,每个共价键属于该C原子的1/2,4.8g石墨的物质的量是4.8g/12g/mol=0.4mol,所以0.4mol石墨晶体中含有共价键是0.4mol×3/2×NA=0.6NA,产物;B、标准状况下11.2L混合气体的物质的量是11.2L/22.4L/mol=0.5mol,CO和N2都是双原子分子,所以含有的原子总数是0.5mol×2×NA=NA,正确;C、羟基中含有8+1=9个电子,而氢氧根离子中含有10个电子,所以1mol的羟基(-OH)与1mol的氢氧根离子(OH-)所含电子数不相同,产物;D、二氧化硫与氧气反应生成三氧化硫,是可逆反应,反应不会进行彻底,所以充分反应后的生成物分子数小于NA,产物,答案选B。
考点:考查阿伏伽德罗常数与微粒数关系的判断
本题难度:一般
2、选择题 设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.在反应5NH4NO3 2HNO3+4N2↑+9H2O中,每生成4 mol N2,转移电子数为10NA
2HNO3+4N2↑+9H2O中,每生成4 mol N2,转移电子数为10NA
B.12.5 mL 16 mol・L-1浓硫酸与足量铜反应,转移电子数为0.2NA
C.标准状况下,1.12L的SO3所含的原子数约为0.2NA
D.标准状况下,2.2gCO2气体中所含分子数为0.05NA
参考答案:D
本题解析:
试题分析:A、每生成4 mol N2,转移电子数为15NA,错误;B、随着反应的进行,浓硫酸渐渐变成稀硫酸
就不再和铜发生反应,所以转移电子数小于0.2NA,错误;C、标准状况下,三氧化硫是固体,错误;D、正确。
本题难度:一般
3、选择题 在T℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g・cm-3,溶质的质量分数为w,其中含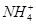 的物质的量为b mol。下列叙述中正确的是( )
的物质的量为b mol。下列叙述中正确的是( )
A.溶质的质量分数为w=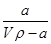 ×100%
×100%
B.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w
C.溶液中c(OH-)=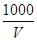 mol・L-1
mol・L-1
D.溶质的物质的量浓度c=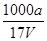 mol・L-1
mol・L-1
参考答案:D
本题解析:溶液的质量是Vρg,所以溶质的质量分数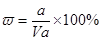 ,A不正确;氨水的密度小于水的,所以上述溶液中再加入V mL水后,所得溶液溶质的质量分数小于0.5w,B不正确;溶液中OH-的物质的量大于bmol,浓度大于
,A不正确;氨水的密度小于水的,所以上述溶液中再加入V mL水后,所得溶液溶质的质量分数小于0.5w,B不正确;溶液中OH-的物质的量大于bmol,浓度大于 本题难度:一般
本题难度:一般
4、选择题 设nA为阿伏加德罗常数的数值,下列说法正确的是
A.3mol NO2与水充分反应,转移nA个电子
B.常温常压下,18g H2O含有3nA个原子
C.1L 0.1 mol・L-1NaHCO3溶液中含有0.1nA个HCO3-
D.标准状况下,2.24L乙醇含有0.1nA个CH3CH2OH分子
参考答案:B
本题解析:
试题分析:A、根据反应3NO2+H2O=2HNO3+NO可知3个NO2分子中有2个NO2中的N由+4价升高到+5价,有1个NO2中的N由+4价降低到+2价,故3mol NO2与水充分反应,转移2nA个电子,故A错误;B、根据n=m/M=18g/18g/mol=1mol,1个H2O中含有3个原子,故常温常压下,18g H2O含有3nA个原子,故B正确;C、NaHCO3中的HCO3-即能电离HCO3- 本题难度:一般
本题难度:一般
5、填空题 (6分)(1)0.3mol NH3分子中所含质子数与 mol H2O分子中所含质子数相等。
(2)已知16克A和20克B恰好完全反应生成0.04mol C和32克D,则C的摩尔质量为________。
(3)如果a g 某气体中含有的分子数为b,则c g 该气体在标准状况下的体积为 L(NA表示阿伏加德罗常数的数值)。
参考答案:(1) 0.3 (2)100g/mol (3)![]()
本题解析:
试题分析:(1)NH3和H2O质子数相同。
(2)根据质量守恒定律得生成C的质量为4g,C的摩尔质量为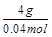 =100g/mol。
=100g/mol。
(3)ag气体中分子数为b,cg气体分子数为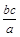 ,气体物质的量为
,气体物质的量为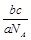 mol,标准状况下气体体积为
mol,标准状况下气体体积为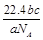 L。
L。
考点:化学计算
点评:n=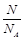 =
= =
=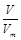
本题难度:一般