微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 在化学反应中,只有极少数 91exam.org能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子。使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ・mol-1表示。请认真观察下图,然后回答问题。
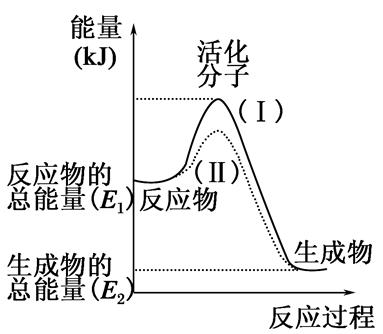
(1)图中所示反应是________(填“吸热”或“放热”)反应。
(2)已知拆开1mol H―H键、1mol I―I、1mol H―I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由1mol氢气和1mol 碘反应生成HI会________(填“放出”或“吸收”)________kJ的热量。在化学反应过程中,是将______转化为________。
(3)下列反应中,属于放热反应的是________,属于吸热反应的是________。
①物质燃烧
②炸药爆炸
③酸碱中和反应
④二氧化碳通过炽热的碳
⑤食物因氧化而腐败
⑥Ba(OH)2・8H2O与NH4Cl反应
⑦铁粉与稀盐酸反应
参考答案:(1)放热 (2)放出 11 化学能 热能
(3)①
本题解析:(1)由图可知反应物的总能量高于生成物的总能量,故该反应为放热反应。
(2)H2(g)+I2(g)=2HI(g),断裂1mol H―H键和1mol I―I 需要吸收436kJ+151kJ=587kJ热量,生成2mol HI放出2×299kJ=598kJ热量,所以1mol 氢气和1mol碘反应生成HI放出11kJ的热量;在化学反应过程中,将化学能转化为热能。
(3)应熟悉常见的吸热反应和放热反应:中和反应、燃料的燃烧、有氧参与的氧化还原反应、多数化合反应等属于放热反应;多数分解反应(H2O2分解除外)、二氧化碳通过炽热的碳、Ba(OH)2・8H2O与NH4Cl反应等属于吸热反应。
本题难度:一般
2、选择题 下列反应的离子方程式不正确的是
A.碳酸氢钠的水解反应:HCO3-+H2O?CO32-+H3O+
B.在碘化亚铁溶液中通入少量氧气:4I-+O2+4H+=2I2+2H2O
C.Cu(OH)2的悬浊液中滴入少量Na2S溶液:Cu2++S2-=CuS↓
D.在氢氧化钡溶液中滴加碳酸氢钡溶液至pH=7:Ba2++OH-+HCO3-=BaCO3↓+H2O
参考答案:AC
本题解析:分析:A.水解生成碳酸;
B.少量氧气,优先氧化碘离子;
C.发生沉淀的转化;
D.pH=7,恰好反应生成碳酸钡和水.
解答:A.碳酸氢钠的水解反应的离子反应为HCO3-+H2O?H2CO3+OH-,故A错误;
B.在碘化亚铁溶液中通入少量氧气的离子反应为4I-+O2+4H+=2I2+2H2O,故B正确;
C.Cu(OH)2的悬浊液中滴入少量Na2S溶液的离子反应为Cu(OH)2+S2-=CuS↓+2OH-,故C错误;
D.在氢氧化钡溶液中滴加碳酸氢钡溶液至pH=7的离子反应为Ba2++OH-+HCO3-=BaCO3↓+H2O,故D正确;
故选AC.
点评:本题考查离子反应的书写,注意反应的实质为解答的易错点,明确生成物及离子反应的书写方法即可解答,选项B中优先氧化为解答的难点,题目难度不大.
本题难度:简单
3、选择题 已知H2O(g) H2O(l)?ΔH=Q1 kJ・mol-1
H2O(l)?ΔH=Q1 kJ・mol-1
C2H5OH(g)  C2H5OH(l)?ΔH=Q2 kJ・mol-1
C2H5OH(l)?ΔH=Q2 kJ・mol-1
C2H5OH(g)+3O2(g) 2CO2(g)+3H2O(g)?ΔH=Q3 kJ・mol-1
2CO2(g)+3H2O(g)?ΔH=Q3 kJ・mol-1
若使23 g液体酒精完全燃烧,最后恢复到室温,则放出的热量为__________kJ(???)
A.Q1+Q2+Q3
B.0.5(Q1+Q2+Q3)
C.0.5Q1-1.5Q2+0.5Q3
D.1.5Q1-0.5Q2+0.5Q3
参考答案:D
本题解析:
试题分析:根据盖斯定律可知,③-②+①×3即得到C2H5OH(l)+3O2(g) 2CO2(g)+3H2O(l),则该反应的热化学方程式△H=(3Q1+Q3-Q2)kJ/mol 。23g酒精的物质的量是23g÷46g/mol=0.5mol,所以若使23 g液体酒精完全燃烧,最后恢复到室温,则放出的热量为(
2CO2(g)+3H2O(l),则该反应的热化学方程式△H=(3Q1+Q3-Q2)kJ/mol 。23g酒精的物质的量是23g÷46g/mol=0.5mol,所以若使23 g液体酒精完全燃烧,最后恢复到室温,则放出的热量为(
本题难度:一般
4、选择题 在[Co(NH3)6]3+中,与中心离子形成配位键的原子是???????(???)
A.N原子
B.H原子
C.Co原子
D.N、H两种原子同时
参考答案:A
本题解析:
试题分析:氢原子不存在孤对电子,但N原子存在孤对电子,所以在[Co(NH3)6]3+中,与中心离子形成配位键的原子是N原子,答案选A。
点评:该题的关键是明确配位健的含义以及形成条件,然后结合原子的结构特点灵活运用即可,有利于调动学生的学习兴趣,提高学生的应试能力。
本题难度:简单
5、选择题 下列过程中△H大于零的是 ( )
A.乙醇燃烧
B.酸碱中和反应
C.碳酸钙分解得二氧化碳
D.实验室制备氢气
参考答案:C
本题解析:A乙醇燃烧是放热反应,△H小于零
B酸碱中和反应是放热反应,△H小于零
C.碳酸钙分解得二氧化碳是吸热反应,△H大于零
D. 实验室制备氢气是放热反应,△H小于零。
本题难度:一般