微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
实验题 在化学分析中,为了测定某试样中FeSO4・7H2O的质量分数,一般采用在酸性条件下用高锰酸钾标准溶液滴定的方法,反应原理为:5Fe2+ +8H+ + MnO4-=5Fe3+ +Mn2+ +4H2O。
高锰酸钾标准溶液可用性质稳定、相对分子质量较大的基准物质草酸钠[Mr(Na2C2O4)=134.0]进行标定,反应原理为:5C2O42- +2MnO4-+16H+=10CO2↑+2Mn2+ +8H2O
实验步骤如下:
步骤一:先粗配浓度约为1.5×10-2 mol・ L-1的高锰酸钾溶液500 mL。
步骤二:称取Na2C2O4固体m g放入锥形瓶中,用蒸馏水溶解并加稀硫酸酸化,加热至70~80℃,用步骤一所配高锰酸钾溶液进行滴定,从而可标定高锰酸钾溶液的浓度。经标定c(KMnO4)=1.6×10-2 mol・L-1。
步骤三:称取FeSO4・7H2O试样1.073 g,放人锥形瓶中,加入适量的水溶解。
步骤四:用标准高锰酸钾溶液滴定步骤三所配样品溶液,达到终点时消耗标准溶液48.00 mL。
试回答下列问题:
(1)步骤一中要用到的玻璃仪器是烧杯、____、____。
(2)步骤二中需要对m的大致值进行预估,你预估的依据是________________。
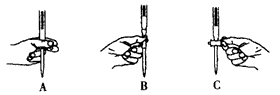
(3)本实验中操作滴定管的以下图示,正确的是____ ______(填编号)。
(4)步骤二的滴定是在一定温度下进行的,操作过程中发现前一阶段溶液褪色较慢,中间阶段褪色明显变快,最后阶段褪色又变慢。试根据影响化学反应速率的条件分析,溶液褪色明显变快的原因可能是_____________。
(5)请设步骤二中的数据记录和数据处理表格__________(不必填数据)。
(6)国家标准规定FeSO4・7H2O的含量(w):
一级品100. 5%≥w≥99.50%;
二 级品100.5%≥w≥99.00%;
三级品101.0%≥w≥98.00%。
试判断该试样符合国家___________级品标准。
(7)测定试样中FeSO4・7H2O的含量时,有时测定值会超过100%,其原因可能是_______________。
实验题 在化学分析中,为了测定某试样中FeSO4・7H2O的质量分数,一般采用在酸性条件下用高锰酸钾标准溶液滴定的方法,反应原理为:5Fe2+ +8H+ + MnO4-=5Fe3+ +Mn2+ +4H2O。
高锰酸钾标准溶液可用性质稳定、相对分子质量较大的基准物质草酸钠[Mr(Na2C2O4)=134.0]进行标定,反应原理为:5C2O42- +2MnO4-+16H+=10CO2↑+2Mn2+ +8H2O
实验步骤如下:
步骤一:先粗配浓度约为1.5×10-2 mol・ L-1的高锰酸钾溶液500 mL。
步骤二:称取Na2C2O4固体m g放入锥形瓶中,用蒸馏水溶解并加稀硫酸酸化,加热至70~80℃,用步骤一所配高锰酸钾溶液进行滴定,从而可标定高锰酸钾溶液的浓度。经标定c(KMnO4)=1.6×10-2 mol・L-1。
步骤三:称取FeSO4・7H2O试样1.073 g,放人锥形瓶中,加入适量的水溶解。
步骤四:用标准高锰酸钾溶液滴定步骤三所配样品溶液,达到终点时消耗标准溶液48.00 mL。
试回答下列问题:
(1)步骤一中要用到的玻璃仪器是烧杯、____、____。
(2)步骤二中需要对m的大致值进行预估,你预估的依据是________________。
(3)本实验中操作滴定管的以下图示,正确的是__________(填编号)。

(4)步骤二的滴定是在一定温度下进行的,操作过程中发现前一阶段溶液褪色较慢,中间阶段褪色明显变快,最后阶段褪色又变慢。试根据影响化学反应速率的条件分析,溶液褪色明显变快的原因可能是_____________。
(5)请设步骤二中的数据记录和数据处理表格__________(不必填数据)。
(6)国家标准规定FeSO4・7H2O的含量(w):
一级品100. 5%≥w≥99.50%;
二 级品100.5%≥w≥99.00%;
三级品101.0%≥w≥98.00%。
试判断该试样符合国家___________级品标准。
(7)测定试样中FeSO4・7H2O的含量时,有时测定值会超过100%,其原因可能是_______________。
本题答案:(1)量筒 ;玻璃棒
(2)根据反应的定量关系、滴定
本题解析:
本题所属考点:【实验方案的设计与评价】
本题难易程度:【困难】
If money be not the servant,it will be the master. 不做金钱的主人,便沦为金钱的奴隶.