微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在过氧化钾与水的反应中,其还原产物和氧化产物质量比为(? )
A.7∶4
B.4∶7
C.7∶2
D.2∶7
参考答案:C
本题解析:K2O2与H2O反应:
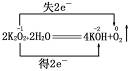
还原产物是KOH,氧化产物是O2,4个KOH中仅有2个是还原产物,故二者质量之比为:2×56∶32=7∶2。
本题难度:简单
2、选择题 钠和铯都是碱金属元素,下列关于铯及其化合物的叙述中不正确的是?:(???)
A.碳酸铯的化学式为Cs2CO3
B.氢氧化铯是一种强碱
C.以电解熔融的CsCl制取铯
D.Cs2CO3加热易分解出CO2、Cs2O
参考答案:D
本题解析:因钠和铯都是碱金属元素性质相似,由Na2CO3知A正确;NaOH为强碱,B正确;制备单质钠常用电解熔融的NaCl的方法,C正确;Na2CO3受热不分解,D错误。答案选D。
本题难度:简单
3、实验题 我国化工专家侯德榜,勇于创新,改进氨碱法设计了“联合制碱法”,为世界制碱工业作出了突出贡献。请完成下列问题:
(1)“联合制碱法”制得的“碱”是??????????????(填化学式)。
(2)氨碱法和联合制碱法是两大重要的工业制碱法,下列表达中,不正确的是??????????。
?
| ?
| 氨碱法
| 联合制碱法
|
A
| 原料
| 食盐、氨气、生石灰
| 食盐、氨气、二氧化碳
|
B
| 可能的副产物
| 氯化钙
| 氯化铵
|
C
| 循环物质
| 氨气、二氧化碳
| 氯化钠
|
D
| 评价
| 原料易得;设备复杂;能耗高
| 原料利用率高;废弃物少
?
某实验小组,利用下列装置模拟“联合制碱法”。
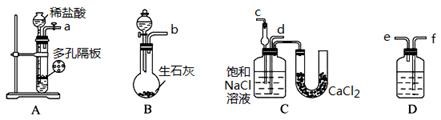
(3)取上述仪器连接装置,顺序为:(a)接(????)、(????)接(????);(b)接(????);
检验气密性后装入药品,应该先让??????????????装置(填上述字母)先发生反应,直到产生的气体不能再在C中溶解时,再通入另一装置中产生的气体。
(4)C中用球形干燥管而不用直导管,其作用是??????????????????????,D中应选用的液体为?????;
(5)C中广口瓶内产生固体的总化学方程式为?????????????????????????????????????。
(6)产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为:???????????????????????(注明你的表达式中所用的有关符号的含义)。
参考答案:(1)Na2CO3
(2)A.C
(3)f? e
本题解析:
试题分析:(1)“联合制碱法”制得的“碱”是碳酸钠,化学式为Na2CO3。
(2)A、氨碱法原料有:食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气,联合制碱法原料有:食盐、氨气、二氧化碳,故A错误;B、氨碱法可能的副产物为氯化钙,联合制碱法可能的副产物氯化铵,故B正确;C、氨碱法循环物质:氨气、二氧化碳,联合制碱法循环物质:氯化钠,二氧化碳,故C错误;D、氨碱法原料(食盐和石灰石)便宜,产品纯碱的纯度高,副产品氨和二氧化碳都可以回收循环使用,制造步骤简单,适合于大规模生产,但设备
本题难度:困难
4、选择题 在相同条件下,总质量为2 g的CO和H2的混合气体,在O2中完全燃烧后全部通过足量的Na2O2固体,则固体质量增加(????)
A.2 g
B.1 g
C.18 g
D.无法计算
参考答案:A
本题解析:CO和氢气燃烧生成CO2和水,通过过氧化钠后,又生成氧气,所以固体增加的质量就是混合气体的质量,即方程式相当于是CO+Na2O2=Na2CO3、H2+Na2O2=2NaOH,答案选A。
本题难度:简单
5、选择题 下列科学家中,为我国化学工业做出重大贡献的是
A.邓稼先
B.李四光
C.华罗庚
D.侯德榜
参考答案:D
本题解析:此题考查了学生的化学史知识。邓稼先是核物理学家,李四光为地质学家,华罗庚为数学家,只有侯德榜为化学家,是侯氏制碱法的发明人。
本题难度:简单
|