微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 图示的装置中,干燥烧瓶中盛有某种气体,烧杯和胶头滴管内盛放同一种溶液。挤压胶头滴管,下列与实验事实不相符的是
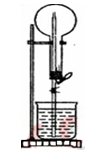
A.CO2(NaHCO3溶液)产生喷泉,得到无色溶液
B.NH3(H2O含酚酞) 产生喷泉,得到红色溶液
C.SO2(品红稀溶液) 产生喷泉,得到无色溶液
D.HCl(AgNO3溶液) 产生喷泉,得到白色悬浊液
参考答案:A
本题解析:考查喷泉实验。碳酸氢钠溶液不能吸收CO2,因此不能形成喷泉,选项A不正确,其余选项都是正确的,答案选A。
本题难度:一般
2、选择题 下列根据事实所得出的结论中,不正确的是
?
| 事实
| 结论
|
A
| 甲、乙两种有机物具有相同的分子式和不同的结构
| 甲和乙互为同分异构体
|
B
| 相同质量的甲、乙两种有机物(只含C、H或C、H、O元素)完全燃烧时产生相同质量的水
| 甲、乙两种分子中,各元素的原子个数比一定相同
|
C
| 在淀粉溶液中加入淀粉酶,一段时间后取出部分水解液,滴加碘水,不变蓝
| 水解液中已不含有淀粉
|
D
| 不存在两种邻二甲苯
| 苯分子中碳碳键完全相同,而不是单双建交替结构
参考答案:B
本题解析:B不正确,相同质量的甲、乙两种有机物(只含C、H或C、H、O元素)完全燃烧时产生相同质量的水即甲、乙分子中H的质量分数相等,而其他原子则不一定。
本题难度:简单
3、选择题 为测定镀锌铁皮锌镀层的厚度,将镀锌皮与足量盐酸反应,待产生的气泡明显减少时取出,洗涤,烘干,称重。关于该实验的操作对测定结果的影响判断正确的是
A.铁皮未及时取出,会导致测定结果偏小
B.铁皮未洗涤干净,会导致测定结果偏大
C.烘干时间过长,会导致测定结果偏小
D.若把盐酸换成硫酸,会导致测定结果偏大
参考答案:C
本题解析:产生的气泡明显减少时,表明锌反应完,若这时铁皮未及时取出,则铁溶解,会导致测定结果偏大,A错误;铁皮未洗涤干净(表面吸附杂质),烘干时间过长(铁被氧化),则剩余物的质量偏大,导致测定结果偏小,B错误,C正确;D项对结果无影响,错误。
【考点定位】本题考查误差分析。
本题难度:一般
4、选择题 某学生做完实验后,采用以下方法分别清洗所用仪器:①用稀硝酸清洗做过银镜反应的试管;②用酒精清洗做过碘升华的烧杯;③用浓盐酸清洗做过高锰酸钾分解实验的仪器;④用盐酸清洗长期保存过三氯化铁溶液的试剂瓶;⑤用氢氧化钠溶液清洗盛放过苯酚的试管。你认为他的操作……( )
A.②不对
B.③④不对
C.④⑤不对
D.全部正确
参考答案:D
本题解析:清洗仪器的主要任务是将不能或不易溶于水的物质转化为可溶于水的物质,然后用水冲洗掉。
①用稀硝酸清洗做过银镜反应的试管----金属银能与硝酸反应,生成溶于水的硝酸银;
②用酒精清洗做过碘升华的烧杯----碘易溶于酒精;
③用浓盐酸清洗做过高锰酸钾分解实验的仪器----高锰酸钾分解产物中二氧化锰在加热条件下与浓盐酸反应生成可溶性的氯化锰;
④用盐酸清洗长期保存过三氯化铁溶液的试剂瓶----长期存放三氯化铁溶液的试剂瓶内壁上常附有一层氧化铁[请大家思考其,可用稀盐酸洗掉;
⑤用氢氧化钠溶液清洗盛放过苯酚的试管----苯酚与氢氧化钠溶液反应生成易溶于水的苯酚钠。
本题难度:一般
5、实验题 CuSO4・5H2O是铜的重要化合物,有着广泛的应用。以下是CuSO4・5H2O的实验室制备流程图。
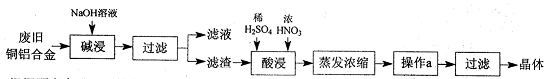
根据题意完成下列填空:
(1)“碱浸”的目的是??????????????????????????????????????????????????????,写出有关的离子方程式??????????????????????????????????????????????????。
(2)向滤渣中先加入足量稀硫酸,然后再滴加少量浓硝酸,在废渣溶解时可以观察到的实验现象有????????????????????????????????????????????????????????????????????????????。
(3)操作a的名称为???????????,制得的CuSO4・5H2O中可能存在硝酸铜杂质,除去这种杂质的实验操作名称为?????????????????。
(4)已知:CuSO4+2NaOH=Cu(OH)2↓+ Na2SO4。称取0.26 g提纯后的CuSO4・5H2O试样于锥形瓶中,加入0.1000 mol/L氢氧化钠溶液28.00 mL,反应完全后,过量的氢氧化钠用0.1000 mol/L盐酸滴定至终点,耗用盐酸8.00 mL,则该试样中CuSO4・5H2O的质量分数为???????;上述滴定中,滴定管在注入盐酸之前,先用蒸馏水洗净,再用???????????????????????。
(5)在“酸浸”的步骤中,①若只加入浓硫酸,写出加热时的化学方程式?????????????????。
②若将浓硝酸换成过氧化氢,常温时即可生成硫酸铜,指出此种方法的优点???????????????。
参考答案:
(1)溶解金属铝、除去油污???? 2Al+2H2O
本题解析:
试题分析:(1)实验目的是利用废旧铝铜合金制备硫酸铜晶体,故应先除杂。碱浸即是除杂过程,除去表面的油污和溶解金属铝,离子方程式为2Al+2H2O+2OH-=2AlO2-+3H2↑;(2)加入少量浓硝酸后稀释,与铜反应,生成硫酸铜和NO气体,故现象为铜溶解,溶液变为蓝色,有无色气体产生并只溶液上方变为红棕色(变成NO2);(3)采用冷却结晶的方法分理出硫酸铜晶体,除去晶体中的可溶性杂质的方法是重结晶;
(4)与CuSO4的氢氧化钠的量n(NaOH)=28.00×0.1000×10-3-8.00
本题难度:一般
|