微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (8分)1994年度诺贝尔化学奖授予为研究臭氧做出贡献的化学家。O3能吸收有害紫外线,保护人类赖以生存的空间。O3的分子结构如图,呈V型,两个O----O键的夹角为116.5o。三个原子以一个O原子为中心,另外两个O原子分别构成一个共价键;中间O原子提供2个电子,旁边两个O原子各提供一个电子,构成一个特殊的化学键------三个O原子均等地享有这4个电子。请回答:?
 ?
?
(1)臭氧与氧气互为____________________,
(2)下列分子中与O3分子的结构最相似的是_____(填选项字母);
A.H2O
B.CO2
C.SO2
D.BeCl2
(3)分子中某原子有一对或几对没有跟其他原子共用的价电子叫孤对电子,那
么O3分子有?????????????对孤对电子。
(4)O3分子是否为极性分子????????????。(填是或否)
(5)O3具有强氧化性,它能氧化PbS为PbSO4而O2不能,试配平:
_____ PbS? +_____ O3? ="===_____" PbSO4 + _____ O2
生成1mol O2的转移电子物质的量为__________ mol。
2、选择题 化学科学需要借助化学专用语言来描述,下列有关化学用语 表示正确的是[???? ]
A.S2-的结构示意图: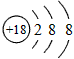
B.N2的电子式: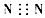
C.次氯酸的结构式:H-O-Cl
D.丙烯醛的结构简式:CH2CHCHO
3、填空题 配位键是一种特殊的共价键,即共用电子对由某原子单方面提供和另一缺电子的粒子结合。如NH4+就是由NH3(氮原子提供电子对)和H+(缺电子)通过配位键形成的。据此,回答下列问题:
(1)下列粒子中可能存在配位键的是________。
A.CO2
B.H3O+
C.CH4
D.H2SO4
(2)硼酸(H3BO3)溶液呈酸性,试写出其电离方程式:___________________。
(3)科学家对H2O2结构的认识经历了较为漫长的过程,最初,科学家提出了种观点:
甲: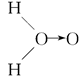 、乙:H―O―O―H,式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:a.将C2H5OH与浓H2SO4反应生成(C2H5)2SO4和水;b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;c.将生成的A与H2反应(已知该反应中H2做还原剂)。
、乙:H―O―O―H,式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:a.将C2H5OH与浓H2SO4反应生成(C2H5)2SO4和水;b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;c.将生成的A与H2反应(已知该反应中H2做还原剂)。
①如果H2O2的结构如甲所示,实验c中化学反应方程式为(A写结构简式)_____________________________________________________________。
②为了进一步确定H2O2的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:____________________________________________________________。
4、选择题 固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体原子的最外层电子层结构,则下列有关说法中,不正确的是( )
A.一个NH5分子中含5个N-H键
B.NH5中既有共价键,又有离子键
C.NH5的电子式是
D.它与HCl反应的离子方程式为NH5+H+=NH4++H2↑
5、选择题 常温下硫单质主要以S8形式存在,加热时S8会转化为S6、S4、S2等,当蒸气温度达到750°C时主要以S2形式存在,下列说法正确的是(? )
A.S8转化为S6、S4、S2属于物理变化
B.不论哪种硫分子,完全燃烧时都生成SO2
C.常温条件下单质硫为原子晶体
D.把硫单质在空气中加热到750°C即得S2