微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将10 mL 5 mol/L 的HCl溶液稀释到 200 mL,从中取出5 mL,这5 mL溶液的物质的
量浓度为
A.0.5 mol/L
B.0.25 mol/L
C.0.1 mol/L
D.1 mol/L
参考答案:B
本题解析:根据稀释定律c1V1=c2V2,c2==0.25mol/L。溶液具有均一性,无论去多少,浓度不变,故答案选B。
本题难度:一般
2、选择题 设NA为阿伏伽德罗常数的值,下列叙述正确的是
A.1 molCl2与足量Fe反应转移电子数一定为3NA
B.标准状况下,2.24 L NH3中含有共价键的数目为NA
C.1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3 NA
D.标况下,11.2 L HF所含的分子数目为0.5NA
参考答案:C
本题解析:
试题分析:A.1 molCl2与足量Fe反应转移电子数为2NA,错误。B一个氨气分子中含有3个共价键,标准状况下,2.24 L NH3的物质的量为0.1mol,中含有共价键的数目为0.3NA。错误。C一个氧化钠或一个过氧化钠中含有的阴离子、阳离子总数为3个离子,所以1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3 NA正确。D在HF分子间存在氢键,通常以聚合分子的形式存在。所以标况下,11.2 L HF所含的分子数目大于0.5NA。错误。
本题难度:一般
3、选择题 废水中CrO42-浓度降至5.0×10-7 mol・L-1以下才能排放。含CrO42-的废水可用沉淀法处理:加入可溶性钡盐生成BaCrO4沉淀,再加入可溶性硫酸盐处理多余的Ba2+。加入可溶性钡盐后的废水中Ba2+的浓度应不小于(已知:Ksp(BaCrO4)=1.2×10-10)
A.1.2×10-5 mol・L-1
B.2.4×10-4 mol・L-1
C.3.6×10-4 mol・L-1
D.4.8×10-4 mo l・L-1
l・L-1
参考答案:B
本题解析:略
本题难度:简单
4、选择题 在相同的温度和压强下,4个容器中分别装有4种气体。已知各容器中的气体和容器的容积分别是a.CO2,100 mL;b.O2,200 mL;c.N2,400 mL;d.CH4,600 mL,则4个容器中气体的质量由大到小的顺序是( )
A.a>b>c>d
B.b>a>d>c
C.c>d>b>a
D.d>c>a>b
参考答案:C
本题解析:
试题分析:设在该温度和压强下,气体的气体摩尔体积为Vm,设在该温度和压强下,气体的气体摩尔体积为Vm,a容器内气体的质量为:m(CO2)= =
= g;b容器内气体的质量为:m(O2)=
g;b容器内气体的质量为:m(O2)= =
=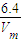 g;c容器内气体的质量为:m(N2)=
g;c容器内气体的质量为:m(N2)=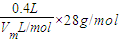 =
= g;d容器内气体的质量为:m(CH4)=
g;d容器内气体的质量为:m(CH4)=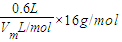 =
=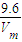 g,则4个容器中气体的质量由大到小的顺序是c>d>b>a.
g,则4个容器中气体的质量由大到小的顺序是c>d>b>a.
考点:阿伏伽德罗常数
本题难度:一般
5、填空题 将0.1molMg、Al混合物溶于100mL4mol/L的盐酸中,然后再滴加1mol/L的NaOH溶液,在滴加NaOH溶液的过程中,沉淀质量m与NaOH溶液的体积V的变化如图所示。
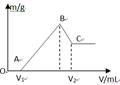
(1)写出BC过程的离子反应方程式????????????????????????????????
(2)当V1=140mL时,混合物中n(Mg)=_____mol,V2=_____mL
(3)滴入的NaOH溶液_____mL时,溶液中的Mg2+和Al3+刚好沉淀完全。
(4)若混合物中Mg的物质的量分数为a,当滴入的NaOH溶液为450mL时,所得沉淀中无Al(OH)3,则a的取值范围是____________________
(5)当加入V2 mlNaOH溶液后过滤,向滤液中通入过量的CO2气体,能观察到的现象为??????????????????,写出该过程反应的离子方程式???????????????????????。
参考答案:(1)Al(OH)3 + OH-? ==AlO2- +2H2
本题解析:
试题分析:(1)由图可以知道,刚开始为酸碱中和,从V1开始,边有沉淀生成,而由于氢氧化铝为两性物质,故BC过程的离子反应方程式为:Al(OH)3 + OH-? ==AlO2- +2H2O;(2)当V1=140mL时,则与镁铝反应的盐酸的量n=0.1×4-0.14×1=0.26mol,设镁为amol,铝为bmol,即a+b=0.1,2a+3b=0.26,联立解得a=0.04,b=0.06,所以混合物中n(Mg)=0.04mol,即从V1到V2所需要的氢氧化钠的物质的量n=0.04×2+0.06×4=
本题难度:一般