微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述不正确的是( )
A.工业上电解饱和食盐水的阳极反应:2Cl--2e-=Cl2↑
B.铁船船体上镶嵌锌块,锌作负极,以防船体被腐蚀
C.钢铁吸氧腐蚀的正极反应:O2+2H2O+4e-=4OH-
D.某同学用右图所示装置完成反应:2HCl+2Ag=2AgCl↓+H2↑
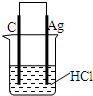
参考答案:A、工业上电解饱和食盐水时,溶液中氯离子的放电能力大于氢氧根
本题解析:
本题难度:简单
2、填空题 I.1100℃时,在恒容密闭容器中,发生如下可逆反应: Na2SO4(s)+4H2(g)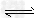 Na2S(s)+4H2O(g),并达到平衡。请完成下列各题:
Na2S(s)+4H2O(g),并达到平衡。请完成下列各题:
(1)达到平衡时的平衡常数表达式:K=________;降低温度,K值减小,则正反应为_________(填“吸热”或“放热”)反应。
(2)向该容器中分别加入以下物质,对平衡的影响如何?
①加入少量Na2SO4,则平衡____________(填所选字母,下同);
②加入少量灼热的Fe3O4,则平衡_____________。
a.正向移动??b.逆向移动??c.不发生移动
Ⅱ.将CH4设计成燃料电池,其利用率更高,装置示意如图 (A、B为多孔性碳棒),持续通入甲烷,在标准状况下,消耗甲烷体积VL。????
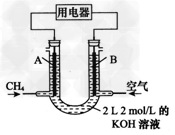
(1)0<V≤44.8?L时,电池总反应方程式为_____________; ??
(2)44.8?L<V≤89.6?L时,负极的电极反应式为__________; ??
(3)V?=67.2?L时,溶液中阴离子浓度大小关系为________________
参考答案:Ⅰ.?(1)c4?(H2O)/c4?(H2)??;吸热 ;a
本题解析:
本题难度:一般
3、选择题 目前人们正在研究开发一种高能电池――钠硫电池,它是以熔融的钠、硫为两极,以能使Na+自由通过而导电的β-Al2O3陶瓷作固体电解质,电池反应为2Na+xS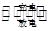 Na2Sx。回答下列问题:
Na2Sx。回答下列问题:
电池在工作时,正极反应式为 ;
负极反应式为 。
参考答案:xS+2e-=Sx 2-
本题解析:正极发生还原反应,单质硫被还原,反应式为xS+2e-=Sx 2-,负极发生氧化反应,钠被氧化,反应式为2Na-2e-=2Na+
本题难度:一般
4、选择题 下列叙述不正确的是:
A.用反应热数据的大小判断不同反应反应速率的快慢
B.用pH数据推测相同浓度的不同强酸弱碱盐在水溶液中水解程度的大小
C.应用盖斯定律,可计算某些难以直接测量的反应焓变
D.用平衡常数的大小判断化学反应可能进行的程度
参考答案:A
本题解析:
试题分析:在相同的外界条件下不同的物质的反应热不同,反应速率可能不同;同一物质在不同的条件下,反应也有快有慢,因此不能用反应热数据的大小判断不同反应反应速率的快慢。符合题意。正确。B.盐的水解规律是:有弱才水解,谁弱谁水解,谁强显谁性。越弱越水解。都强不水解。所以可根据用pH数据推测相同浓度的不同强酸弱碱盐在水溶液中水解程度的大小。不符合题意。错误。C.盖斯定律可知:反应热与反应的途径无关,而只与物质的开始状态与终了状态有关。因此可利用盖斯定律不仅能够直接测量某些反应的反应热,也可计算某些难以直接
本题难度:一般
5、填空题 下图为氢氧燃料电池原理示意图,请根据提示写出正负极的电极反应式
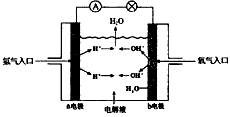
(1) 以硫酸为电解液:负极:________________正极:________________
(2) 以氢氧化钾为电解液:负极:____________________正极:___________________
参考答案:(1)2H2-4e-==4H+;O2+4H++4e-==2H
本题解析:
本题难度:一般