��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� I��ﮡ�����������ܹ��ṩ�൱����ͨ����ӵ��10����������������Ǻ���ǰ;�ĵ�ؼ�������ͼ��ﮡ���������طŵ�ʱ�Ĺ���ʾ��ͼ��
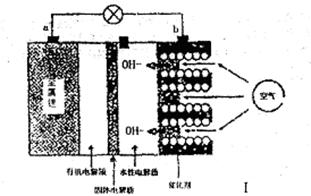
��1��ͼ1�е缫a��??????????????����
��2������м�Ĺ������ʣ��������ӽ���Ĥ��������ֹH2O��N2��O2�����ʵ�ͨ����ֹLi����Щ���ʷ�Ӧ��Li��ˮ�ڳ����·�����Ӧ�Ļ�ѧ����ʽΪ?????????????????????��
II��ijЩ﮵�ع㷺Ӧ�����ֻ��������������Яʽ�����С�����﮵�صĸ���ͨ���ɽ���﮹��ɣ������ɶ���������SOCl2����̼���Ϲ��ɡ��ܷ�ӦΪ��4Li+2SOCl2=4LiCl+S+SO2��������﮵����һ�ε�أ��ڷŵ�ʱ���������������˵������ȷ����????????????????��
A���ŵ�ʱ����ڲ�Li+���ƶ�[
B���ŵ�����У���ظ�������������Ӧ
C���ŵ�ʱÿ�ƶ�2mol���ӣ���1molS����ԭ
D���ŵ�ʱ���������ӦΪ ��3SOCl2+4e-=SO2+S+4Cl-
��3SOCl2+4e-=SO2+S+4Cl-
III��﮵�ػ��վ�����Ҫ���壬�ص���յ��������ϣ�����Ҫ�ɷ�Ϊ����ﮣ�LiCoO2���������ȡ�
ij���չ����������£�
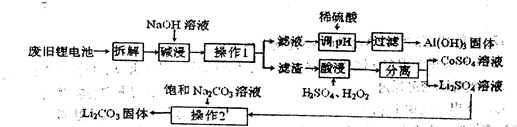
��1���Ͼɵ�ز����е���ﮣ����ʱ���������������Ϊ���������е�?????? ???��Ӧ��
???��Ӧ��
��2�����ʱ����﮷�����Ӧ�Ļ�ѧ����ʽΪ???????????????????�������������H2SO4��H2O2���ҺҲ�ܴﵽ���Ŀ�ģ�������֮����????????????��
��3��Li2CO3��ˮ�е��ܽ�����¶����߶���С������2�IJ����ǣ�����Ũ���������塢???��ϴ�ӡ����
�ο��𰸣� �����������
�����������
�����Ѷȣ�һ��
2��ѡ���� �ݱ�������ȼ�ϵ�ع������Ѿ�ʻ�ϱ�����ͷ������˵����ȷ����[???? ]
A�����ˮ��ȡ��������������õ����ⷽ��
B����չ��ȼ�ϵ��������Ҫ��ȫ��Ч�Ĵ��⼼��
C��Ѱ�Ҹ�Ч������ʹˮ�ֽ��������ͬʱ�ͷ�����
D����ȼ�ϵ���ǰ�����������ȼ�շų�������ת��Ϊ����
�ο��𰸣�B
���������
�����Ѷȣ���
3������� ��15�֣�I.�о����������������ڴ����к������ӵ������ʱ��ͬ�¶����漰���·�Ӧ��
a��2NO��g��+Cl2��g��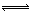 2ClNO��g�� ?H1<0 ��ƽ�ⳣ��ΪK1
2ClNO��g�� ?H1<0 ��ƽ�ⳣ��ΪK1
b��2NO2��g��+NaCl��s��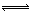 NaNO3��s��+ClNO��g�� ?H2<0 ��ƽ�ⳣ��ΪK2
NaNO3��s��+ClNO��g�� ?H2<0 ��ƽ�ⳣ��ΪK2
��1��4NO2��g��+2NaCl��s�� 2NaNO3��s��+2NO��g��+Cl2��g�� ?H3��ƽ�ⳣ��K= ����K1��K2��ʾ����?H3= ����?H1��?H2��ʾ����
2NaNO3��s��+2NO��g��+Cl2��g�� ?H3��ƽ�ⳣ��K= ����K1��K2��ʾ����?H3= ����?H1��?H2��ʾ����
��2��Ϊ�о���ͬ�����Է�Ӧa��Ӱ�죬�ں��������£���2L�����ܱ������м���0.2mol NO��0.1mol Cl2��10minʱ��Ӧa�ﵽƽ�⡣���10min�ڦԣ�ClNO��=7.5��10��3mol?L-1?min��1����ƽ���n��Cl2��= mol��NO��ת���ʦ�1= �������������ֲ��䣬��Ӧ��1���ں�ѹ�����½��У�ƽ��ʱNO��ת����Ϊ��2����1 ��2���>����<����=������ƽ�ⳣ��K1 ���������С�����䡱������ҪʹK1��С���ɲ��õĴ�ʩ�� ��
II.��������϶�����Ŀǰһ��ʹ�������أ��õ�������Ļ�����Ϊ�����������������M��ʾ��Ϊ��������Һ����ҪΪKOH��Ϊ�������Һ�������س�ŵ�ԭ��ʾ����ͼ��
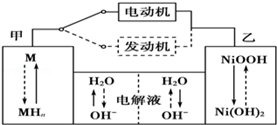
���ܷ�ӦʽΪH2+2NiOOH 2Ni(OH)2 ������������Ϣ�жϣ���϶��������»����ʱ���缫��Χ��Һ��pH ���������С�����䡱���� �ҵ缫�ĵ缫��Ӧʽ ��
2Ni(OH)2 ������������Ϣ�жϣ���϶��������»����ʱ���缫��Χ��Һ��pH ���������С�����䡱���� �ҵ缫�ĵ缫��Ӧʽ ��
�ο��𰸣�I��1��K22/ K1, 2?H2-
���������
�����Ѷȣ�����
4��ѡ���� ����������ѧ��������һ�����͵��Ҵ���أ��������Ե���ʣ�H+�����ܼ�������ܷ�ӦΪ��C2H5OH+3O2=2CO2+3H2O������˵������ȷ���ǣ�������
A���Ҵ��ڵ�صĸ����ϲμӷ�Ӧ
B��1mol?CH3CH2OH������ת��6mol����
C�������·�е����ɸ����ص�����������
D����������ĵ缫��ӦΪ4H++O2+4e-��2H2O
�ο��𰸣�A���ɷ�Ӧ���ܷ���ʽ��֪�Ҵ����������ڸ�����ʧȥ���ӣ���A��
���������
�����Ѷȣ�һ��
5��ѡ���� ���Ӽ��������õ�Ŧ�۵���У���ԭ����п����������Ag2O���������ҺΪKOH��Һ����缫��Ӧ���£�Zn-2e-+2OH-�TZnO+H2O��Ag2O+2e-+H2O�T2Ag+2OH-��
����������ȷ���ǣ�������
A��пΪ����
B���ŵ�ʱ����������Һ��pH����
C��пΪ����
D���ŵ�ʱ����������Һ��pH��С
�ο��𰸣�A�����ݻ��ϼ۱仯��֪Zn��������ӦΪԭ��صĸ�����������Ϊ
���������
�����Ѷȣ���