微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (15分)NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品,工业上常用铝土矿(主要成分为Al2O3和少量的 SiO2、Fe2O3杂质)生产铵明矾晶体
NH4Al(SO4)2?12H2O,其工艺流程图如下:

(1)废渣a、b 的成分分别是:_________、_____________。(写名称)
(2)流程图中X的化学式为:_______________。
(3)反应Ⅲ的离子方程式为:_________________________________________;从铵明矾溶液中获得铵明矾晶体的操作依次为(填操作名称)_________、冷却结晶、过滤洗涤。
(4)过硫酸铵[(NH4)2S2O8]在工业生产中有广泛的用途,可以作为氧化剂和漂白剂,广泛地用于蓄电池工业;还用作聚合的引发剂、纤维工业的脱浆剂。在上述的工艺流程中用惰性电极电解X与反应Ⅵ所得物质的混合溶液可以得到过硫酸铵。
写出阳极反应式:________________________ ____。
(5)反应Ⅶ的化学方程式为:_________________________ _____________;
NH4HSO4溶液中离子浓度由大到小顺序为:__________________________ _。
(6)向硫酸铝铵溶液中逐滴加入氢氧化钡溶液,不可能发生的反应是 (填选项字母)
A.4NH4Al(SO4)2+3Ba(OH)2=2(NH4)2SO4+3BaSO4↓+ Al2 (SO4)3+2Al(OH)3↓
B.2NH4Al(SO4)2+4Ba(OH)2=(NH4)2SO4+3BaSO4↓+Ba(AlO2)2
C.2NH4Al(SO4)2+3Ba(OH)2=(NH4)2SO4+3BaSO4↓+2Al(OH)3↓
D.NH4Al(SO4)2+2Ba(OH)2=NH3・H2O+2BaSO4↓+ Al(OH)3↓
参考答案:(1)二氧化硅(1分)、氢氧化铁(1分)
(2)H2S
本题解析:
试题分析:根据铝土矿的成分和流程图中反应III通入CO2,可推知X为H2SO4,Y为NaOH。
(1)铝土矿加入过量硫酸溶液,得到的废渣a为:二氧化硅;再通入过量的NaOH溶液,Fe2(SO4)3与NaOH反应得到的废渣b为:氢氧化铁。
(2)根据上述分析,流程图中X的化学式为:H2SO4
(3)由工艺流程转化可知,反应III为向含有AlO2-的的滤液中通入过量CO2气体,使AlO2-完全转化为Al(OH)3,在溶液中CO2、AlO2-、H2O反应生成Al(OH)3与HCO3-,反应离子方程式为AlO2-+CO2+2H2O=HCO3-+Al(OH)3↓;从铵明矾溶液中获得铵明矾晶体的操作依次为:蒸发浓缩、冷却结晶、过滤洗涤。
(4)根据电解原理阳极失电子发生氧化反应,SO42?失电子生成S2O82-,电极方程式为:2SO42--2e-
本题难度:困难
2、填空题 已知以下两个氧化还原反应的化学方程式:
①Cl2+H2O===HCl+HClO ②2Al+Fe2O3 Al2O3+2Fe
Al2O3+2Fe
(1)用单线桥法表示反应②中的电子转移情况:______。
(2)若反应②中每生成1 mol Fe,转移电子的物质的量是:________。
(3)将反应①改写成离子方程式:________。
参考答案:22.(1) 本题解析:
本题解析:
试题分析:(1)单线桥法中的箭头由还原剂指向氧化剂,在第二个反应中,Al作还原剂,Fe2O3作氧化剂,其中的Fe被还原,表示为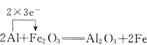 ;
;
(2)铁元素由+3价降低到0价,转移3个电子,每生成1 mol Fe,转移电子的物质的量是3mol;
(3)将反应①改写成离子方程式为Cl2+H2O===H++Cl-+HClO。
考点:考查氧化还原反应。
本题难度:一般
3、填空题 (6*1分)某溶液中含有SO42-、CO32-、Cl-三种阴离子。如果每次只检验一种离子,要↑
(1)先检验CO32-,加入 试剂(或溶液),反应的离子方程式为 ;
(2)然后检验SO42,加入 试剂(或溶液),反应的离子方程式为 ;
(3)最后检验Cl-,加入 试剂(或溶液),反应的离子方程式为 。
参考答案:见解析。
本题解析:试题分析:.因为要求每次只检验其中一种离子,应注意试剂添加顺序。(1)先检验CO32-,加入稀硝酸,反应的离子方程式为2H++CO32-=CO2↑+H2O;(2)然后检验SO42,加入Ba(NO3)2溶液,反应的离子方程式为Ba2++SO42-=BaO4↓;(3)最后检验Cl-,加入AgNO3溶液,反应的离子方程式为Ag++Cl-=AgCl↓;
考点:了解离子反应的概念、离子反应发生的条件。了解常见离子的检验方法。
点评:本题考查常见离子的检验,当溶液中存在多个离子需要检验时,就注意离子间的相互干扰,检验试剂的添加要有一定顺序。
本题难度:一般
4、填空题 (10分)霞石是一种硅酸盐,其组成可表示为K2O・3Na2O・4Al2O3・8SiO2,某小组同学设计以霞石为原料制备Al2O3的方案如下:
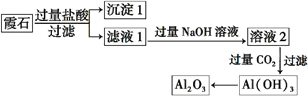
请回答下列问题:
(1)沉淀1的主要成分的化学式为 。
(2)向滤液1中加入过量NaOH溶液的有关反应离子方程式为 。
(3)由溶液2生成Al(OH)3的离子方程式为 。
(4)某同学提出上述流程较繁琐,可简化流程,其方法是向滤液1中加入足量的试剂X即可得到Al(OH)3,则试剂X为 。
参考答案:(1) SiO2 (2分)
(2
本题解析:
试题分析:霞石(K2O・3Na2O・4Al2O3・8SiO2)加入过量盐酸后SiO2不溶转化为沉淀1,其他成分转化为KCl、NaCl、AlCl3、以及过量的盐酸存在滤液1中,滤液1加入过量NaOH溶液后溶液2的成分为KCl、NaCl、NaAlO2、以及过量的NaOH,再通入过量CO2时,生成Al(OH)3沉淀,Al(OH)3受热分解生成Al2O3。(1) 沉淀1的主要成分的化学式为SiO2;(2) 向滤液1中能与过量NaOH反应的物质有AlCl3和盐酸,有关反应离子方程式为:H++OH- = H2O 、Al3++4OH- = AlO2-+2H2O(或Al3++3OH- = Al(OH)3↓ ,Al(OH)3+OH- = AlO2-+2H2O);(3) 过量CO2与溶液2中的NaAlO2反应生成Al(OH)3的离子方程式为:AlO2-+CO2+2H2O = Al(OH)3↓+HCO3-;(4) Al(OH)3可溶于强碱但不溶于弱碱氨水,向滤液1中加入过量的NaOH溶液产生NaAlO2再通入过量CO2产生Al(OH)3,流程繁琐且试剂用量多,若用氨水代替,过量的氨水直接将滤液1中的AlCl3转化为Al(OH)3,故X为氨水。
考点:考查铝的化合物的性质。
本题难度:一般
5、填空题 (9分)盐酸常用于清除金属表面的铜锈铁锈。某同学欲将除锈后的盐酸中的金属元素分步沉淀,查资料获知常温下水溶液中各离子沉淀的pH范围:
离子
| 开始沉淀的pH
| 沉淀完全的pH
|
Fe3+
| 1. 0
| 3. 0
|
Fe2+
| 5. 8
| 8. 8
|
Cu2+
| 4.2
| 6.7
(1)若以离子浓度降至1×10-5 mol・L-1为沉淀完全,根据上表数据推算出ksp[Fe(OH)3]=
(2)根据上述数据该同学设计了以下实验流程:

A可能是 ;试剂B的化学式是 ;沉淀②化学式是 。
参考答案:(共9分):(1)1.0×10-38(3分)
(2)双
本题解析:
试题分析:(1)根据表格的数据可知Fe3+沉淀完全的溶液的pH="3." 0, c(OH-)=10-11,离子浓度降至1×10-5 mol・L-1为沉淀完全,则ksp[Fe(OH)3]=c(Fe3+)?c3(OH-)=1×10-5×(10-11)3=1×10-38; (2)向含有Fe3+、Fe2+、Cu2+的盐酸溶液中加入双氧水等氧化剂,会把Fe2+氧化为Fe3+,得到含有Fe3+、Cu2+的盐酸溶液,然后向该溶液中加入NaOH溶液,调整溶液的pH=4,这时首先得到Fe(OH)3沉淀,过滤,得到的滤液中再加入NaOH只溶液的pH≥6.7,溶液中的Cu2+就会形成Cu(OH)2沉淀,因此沉淀②是Cu(OH)2。
考点:考查沉淀溶解平衡常数的计算、溶液中杂质离子除去的试剂的选择、沉淀的成分的确定的知识。
本题难度:困难
|