微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (3分)乙酸是食醋的主要成分,它具有以下化学性质:‘
(1)可使紫色石蕊试液变______色,说明乙酸具有______性。
(2)能发生酯化反应。实验室用右图所示装置制取乙酸乙酯,请写出该反应的化学方程式:???????????????????????????????????????。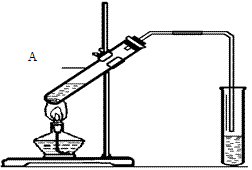
参考答案:(1)红,酸。(2) 本题解析:略
本题解析:略
本题难度:简单
2、选择题 从下列事实所得出的相应结论正确的是
A.A
B.B
C.C
D.D
参考答案:D
本题解析:分析:A、氢氧化铝属于碱,可以和碱反应的物质是酸或是酸性氧化物以及盐等;
B、二氧化碳的水溶液导电是碳酸导电,不是二氧化碳本身导电;
C、二氧化硫具有还原性,能被高锰酸钾氧化;
D、根据氧化剂将金属氧化到的价态来确定氧化性的强弱.
解答:A、氢氧化铝可以溶解在氢氧化钠溶液中,说明氢氧化铝可以和强碱反应,但是不能说明是碱就可以溶于氢氧化钠中,故A错误;
B、CO2的水溶液可导电是碳酸导电,二氧化碳属于非电解质,故B错误;
C、SO2通入酸性高锰酸钾溶液,溶液将二氧化硫氧化,因为发生氧化还原反应而褪色,证明二氧化硫具有还原性,故C错误;
D、铁分别和氯气、硫反应得到氯化铁和硫化亚铁,氯气可以将金属铁氧化到高价,硫将金属铁氧化到低价,所以氯气的氧化性大于硫,故D正确.
故选D.
点评:本题考查学生物质的性质方面的知识,注意知识的积累是解题的关键,难度不大.
本题难度:困难
3、选择题 1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,

反应温度为115℃~125℃,反应装置如右图。下列对该实验的描述错误的 是( )
A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
D.加入过量乙酸可以提高1-丁醇的转化率
参考答案:C
本题解析:
试题分析:A、因此反应需要反应温度为115~125℃,而水浴加热适合温度低于100℃的反应,故A正确;B、有易挥发的液体反应物时,为了避免反应物损耗和充分利用原料,要在发生装置设计冷凝回流装置,使该物质通过冷凝后由气态恢复为液态,从而回流并收集.实验室可通过在发生装置安装长玻璃管或冷凝回流管等实现,故B正确;C、使用氢氧化钠溶液洗涤,会使乙酸乙酯发生水解而使实验失败,故C错误;D、酯化反应为可逆反应,增加乙酸的量,可使平衡向生成酯的方向移动,从而提高1-丁醇的转化率,故D正确。故选C。
本题难度:简单
4、选择题 浓硫酸与铜在加热的条件下反应生成硫酸铜、二氧化硫与水。反应中,浓硫酸所表现的性质有[???? ]
A.只有酸性
B.只有强氧化性
C.脱水性
D.既有强氧化性,又有酸性
参考答案:D
本题解析:
本题难度:简单
5、选择题 以下不符合工业生产事实的是
A.金属铝:冶铁时作还原剂
B.生石灰:炼钢时作造渣材料
C.氨水:制硫酸时吸收尾气中SO2
D.铂铑合金:制硝酸时作催化剂
参考答案:A
本题解析:分析:A、冶炼铁通常利用比较便宜的CO作还原剂;
B、生石灰与二氧化硅反应生成硅酸钙,生成炉渣;
C、用氨水吸收尾气中的SO2,当吸收液中NH4HSO3达到一定浓度后,再与硫酸反应,放出的SO2可用作化工原料,循环利用,生成的硫酸铵可用作肥料;
D、氨的催化氧化利用铂铑合金作催化剂.
解答:A、冶炼铁通常利用比较便宜的C、CO作还原剂,故A不符合;
B、生石灰与二氧化硅反应生成硅酸钙,生成炉渣,故B符合;
C、工业上制取硫酸时排放的尾气中的SO2常采用氨吸收法,即先用氨水吸收尾气中的SO2,当吸收液中NH4HSO3达到一定浓度后,再与硫酸反应,放出的SO2可用作化工原料,循环利用,生成的硫酸铵可用作肥料,故C符合;
D、氨在铂铑合金作催化剂、加热条件下生成NO,NO氧化生成二氧化氮,二氧化氮与水反应可得硝酸,故D符合.
故选A.
点评:本题考查学生对化学工业的掌握,比较基础,旨在考查学生对化学工业工业流程的理解掌握,以考查学生的识记为为主.
本题难度:简单