��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���������������ڴ��������еĵ�����������Ļ�ѧ��ӦΪ��
2NH3(g ) + NO(g) + NO2(g) 2N2(g) + 3H2O(g)
2N2(g) + 3H2O(g)
�ں��ݵ��ܱ������У������й�˵����ȷ���� [???? ]
A��ƽ��ʱ�������������䣬�����¶ȿ�ʹ�÷�Ӧ��ƽ�ⳣ������
B��ƽ��ʱ�������������䣬����NH3��Ũ�ȣ������е��������ת���ʼ�С
C����λʱ��������NO��N2�����ʵ�����Ϊ1��2ʱ����Ӧ�ﵽƽ��
D�������������䣬ʹ�ø�Ч�����������е��������ת��������
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2������� ����10���4��105Pa�������£�����ӦaA��g��?dD��g��+eE��g������ƽ���ά���¶Ȳ��䣬��������ϵ��ѹǿ���ڲ�ͬѹǿ�¸÷�Ӧ����ƽ�������D��Ũ�ȼ��±���������ѹǿ�Ĺ���������������Ӧ��������
| ѹǿ��Pa�� | 4��105 | 6��105 | 1��106 | 2��106
D��Ũ�ȣ�mol/L��
0.085
0.126
0.200
0.440
��ѹǿ��4��105Pa���ӵ�6��105?Paʱƽ��Ӧ��______��Ӧ�����ƶ�����������桱����ͬ����������______��
��ѹǿ��1��106?Pa?���ӵ�2��106?Paʱ��ƽ����______��Ӧ�����ƶ�����ʱƽ����÷����ƶ���������Ҫ������______��______��
����10���1.01��105Pa�������£����ݻ��ɱ���ܱ������г���a?molA��b?molB������Ӧ2A��g��+B��g��?D��g��+E��s������ƽ��������ܶȲ��䣬��֪�����ʵ�Ħ����������λ��g?mol-1���ֱ�ΪA18��B46��D42��E40����a��bΪ______��
����֪T�桢P?kPaʱ�����ݻ��ɱ���ܱ������г���2mol?X��1mol?Y����ʱ�ݻ�ΪV?L�����ֺ��º�ѹ��ʹ��Ӧ��2X��g��+Y��g��?2Z��g���ﵽƽ��ʱ��Z���������Ϊ0.4���������¶���ΪT�棬��ѡһ�ݻ�ΪV?L�Ĺ̶�������ܱ������������г���һ������X��Y��ʹ��Ӧ�ﵽƽ�⣬��ʱZ�����������Ϊ0.4��������X��Y�����ʵ���Ӧ����Ĺ�ϵ�ǣ�a?n��Y����n��X����b?n��Y������aΪ______��
�ο��𰸣���ѹǿ��4��105Pa���ӵ�6��105 Paʱ��D��Ũ��
���������
�����Ѷȣ�һ��
3��ѡ���� ��֪298Kʱ��Ӧ2SO2��g��+O2��g���T2SO3��g����H=-197kJ?mol-1������ͬ�¶�����һ�ܱ������м���2molSO2��1molO2���ﻯѧƽ��ʱ�ų�����Ϊa1kJ������һ�ݻ���ͬ���ܱ�������ͨ��1molSO2��0.5molO2���ﻯѧƽ��ʱ�ų�����Ϊa2kJ�������й�ϵʽ����ȷ���ǣ�������
A��2a2��a1��197
B��2a2��a1��197
C��2a2=a1��197
D��2a2=a1=197
�ο��𰸣���Ӧ���Ȼ�ѧ����ʽΪ��2SO2��g��+O2��g��![]()
���������
�����Ѷȣ�һ��
4��ѡ���� ��ͼ��ʾ��������������ж�����2 mol X��2 mol Y��K�رգ�����ʼV��=0.8a L��V��= aL������ͬ�㶨�¶��£��������и��Է������з�Ӧ��X(g)+Y(g)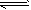 2Z(g)+W(g)���ﵽƽ��ʱ��V��=0.9aL��������˵��������� 2Z(g)+W(g)���ﵽƽ��ʱ��V��=0.9aL��������˵���������
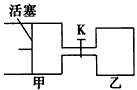 [???? ] [???? ]
A���������дﵽƽ���ʱ�䣺��<��
B����������X��ת����Ϊ25%���ұ���������X��ת����С
C����K�ﵽ��ƽ��ʱ�������������Ϊ0. 8aL����ͨ��������������ƣ�
D����K�ﵽ��ƽ��������������¶ȣ����������һ������
�ο��𰸣�D
���������
�����Ѷȣ�һ��
5������� �̶�������CO2������Ч��������Դ�������ٿ����е��������塣
��.��ҵ�������о�����CO2�������״�ȼ�ϵķ������÷����Ļ�ѧ����ʽ�ǣ�
CO2(g)?+?3H2(g) CH3OH(g)?+?H2O(g)???��H=?-49.0?kJ��mol-1��ij��ѧʵ�齫6?mol?CO2��8?mol?H2����һ�ݻ�Ϊ2L���ܱ������У��¶ȱ��ֲ��䣩�����H2�����ʵ�����ʱ��仯����ͼ1��ʵ����ʾ��ͼ����ĸ������ֱ�ʾ��Ӧ�����꣩�� CH3OH(g)?+?H2O(g)???��H=?-49.0?kJ��mol-1��ij��ѧʵ�齫6?mol?CO2��8?mol?H2����һ�ݻ�Ϊ2L���ܱ������У��¶ȱ��ֲ��䣩�����H2�����ʵ�����ʱ��仯����ͼ1��ʵ����ʾ��ͼ����ĸ������ֱ�ʾ��Ӧ�����꣩��

�ش��������⣺
��1���÷�Ӧ��_____���������Է����У����ţ��� ????
?A������?????B������?????C���κ��¶�
��2���÷�Ӧ��0��8?min��CO2��ƽ����Ӧ������__________��
��3���÷�Ӧ��ƽ�ⳣ��K=__________��
��4�����ı�ijһ�����ٽ���ʵ�飬���H2�����ʵ�����ʱ��仯��ͼ��������ʾ����ʵ����ȣ����ߢ�ı������������_______________����ʵ�߶�Ӧ������ƽ�ⳣ��ΪK�����ߢ��Ӧ������ƽ�ⳣ��ΪK1�����ߢ��Ӧ������ƽ�ⳣ��ΪK2����K��K1��K2�Ĵ�С��ϵ��____________________��
��.��ҵ�ϻ�����CO����ȼ�ϼ״���һ�������·�����Ӧ��CO(g)?+?2H2(g) CH3OH(g)?? CH3OH(g)??
��1��ѡ�����˵Ĵ�����________����ܡ����ܡ�)�ı�÷�Ӧ�ķ�Ӧ�ȣ�
��2�����������£����д�ʩ����ʹ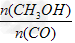 �����_________��?? �����_________��??
a�������¶�????b������He��?? c���ٳ���2mol?H2?????d��ʹ�ô���
��3�����ݻ�ѧ��Ӧ�����뻯ѧƽ�����ۣ���ϵ��������ʵ�ʣ�����Ϊ����˵������ȷ����
________��
A����ѧ��Ӧ�������ۿ�ָ��������һ��ʱ���ڿ����Ʒ
B����Ч��ײ���ۿ�ָ���������ԭ�ϵ�ת����
C����������ԭ����ָ������ʹ������ԭ�϶����Ʒ
D��������ʹ������߲��ʵ���Ч����
E����ȷ���û�ѧ��Ӧ���ʺͻ�ѧ��Ӧ�ȶ�����������������ۺϾ���Ч��
�ο��𰸣���1��B����2��0.125 mol / (L��min)����
���������
�����Ѷȣ�һ��
|