微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 NA代表阿伏加德罗常数,下列说法正确的是(???)
A.如果5.6LN2含有n个氮分子,则阿伏加德罗常数一定约为4n
B.15.6gNa2O2与过量CO2反应时,转移的电子数为0.4NA
C.1L1mol/L的FeCl3溶液中,含有铁离子的数目为NA
D.T℃时,1LPH=6纯水中,含10-6NA个OH-
参考答案:D
本题解析:N2所处的条件不清,A错;2mol Na2O2与过量CO2反应转移2mol电子,故0.2mol Na2O2参与此反应转移0.2mol电子,B错误; Fe3+要发生水解,C错误;D正确。
本题难度:简单
2、选择题 下列溶液中物质的量浓度为1 mol・L-1的是
A.将40 g NaOH溶解于1 L 水中
B.将22.4 L氨气溶于水配成1 L溶液
C.将10 g NaOH溶解在水中配成250 mL溶液
D.将1 L 10 mol・L-1的浓盐酸与9 L水混合
参考答案:C
本题解析:A 错误,应该是溶于水配成1L溶液
B 错误,没有说标况
C 正确
D 错误,1L盐酸和9L水混合体积不是10L,应小于10L
故选C
本题难度:简单
3、选择题 设NA表示阿伏加德罗常数,下列叙述中正确的是?????
A.常温常压下,11.2 L氧气所含的分子数为NA
B.1.8 g的NH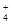 中含有的电子数为NA
中含有的电子数为NA
C.常温常压下,48 g O3含有的氧原子数为NA
D.24 g金属镁变为镁离子时失去的电子数为NA
参考答案:B
本题解析:A.非标准状态,无法计算
B.正确
C.常温常压下,48g O3含有的氧原子数为3NA
D.24 g金属镁变为镁离子时失去的电子数为2NA
故答案为B
本题难度:简单
4、选择题
A.1mol 任何气体单质在标况下体积都约为22.4L,含有的原子数都为2×6.02×1023
B.同温、同压、同体积的氢气和氧气具有相同的分子数
C.在铁与硫的反应中,1mol 铁失去的电子数为3×6.02×1023
D.在pH="13" 的 NaOH 溶液中,OH-的数目为0.1×6.02×1023
参考答案:B
本题解析:阿伏加德罗常数的考查是历年高考热点。本题考查知识点有物质的量,阿伏加德罗定律,氧化还原反应中电子的转移,溶液酸碱性等。A中1mol 任何气体单质含有的原子数都为2×6.02×1023错误,原子数与单质的分子构成有关。C中铁与硫的反应生成FeS,1mol 铁失去的电子数为2×6.02×1023,D中溶液的体积未知无法计算溶质的物质的量。由阿伏加德罗定律知,B正确。
本题难度:一般
5、选择题 NA代表阿伏加德罗常数,下列叙述正确的是
A.1 mol Cl2溶于水的过程中有2NA个电子转移
B.在1 L 0.1 mol・L-1氟化钠溶液中含有F-数目为NA
C.1 mol甲醇中含有C―H键的数目为3NA
D.10 L pH=1的硫酸溶液中含有的H+数目为2NA
参考答案:C
本题解析:
试题分析:氯气与水反应生成次氯酸和氯化氢,氯元素由0价变为―1价和+1价,氯气既是氧化剂又是还原剂,则Cl2+H2O HClO+HCl~e―,由于可逆反应不能进行到底,氯气与转移电子的系数之比等于物质的量之比,则1mol氯气溶于水转移电子小于1mol,故A选项错误;由于c?V=n,则NaF为0.1mol,
HClO+HCl~e―,由于可逆反应不能进行到底,氯气与转移电子的系数之比等于物质的量之比,则1mol氯气溶于水转移电子小于1mol,故A选项错误;由于c?V=n,则NaF为0.1mol,
本题难度:简单