微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (8分)向等体积pH=a的盐酸和pH=b的醋酸溶液中分别加入100 mL pH=12的NaOH溶液,充分反应后,两溶液均呈中性。则:
(1)a与b的关系为a________b(填“大于”、“小于”或“等于”,下同)。
(2)向等体积的该盐酸和醋酸溶液中分别加入足量的锌粉,充分反应后,产生H2的体积关系为V(H2)盐酸________V(H2)醋酸;反应完成所需时间t(HCl)________t(CH3COOH)。
(3)若盐酸的体积为10 mL,则盐酸的物质的量浓度为__________________。
参考答案:(1)小于?(2)小于?小于?(3)0.1 mol・L-1
本题解析:(1)因为醋酸是弱酸,所以其浓度要大于10-b mol・L-1,而盐酸的浓度是10-amol・L-1。若a=b,则反应后醋酸一定是过量的,溶液应该显酸性,但实际是显中性的,所以只能是a小于b,才有可能使反应后的溶液均显中性。
(2)因为醋酸的浓度要大于盐酸的浓度,因此在溶液体积相等的条件下,醋酸产生的氢气多。
(3)根据盐酸和氢氧化钠反应后的溶液显中性,可计算,即0.01L×10-amol/L=0.1L×0.01mol/L,解得a=1,所以其浓度是0.1 mol・L-1。
本题难度:一般
2、选择题 下列说法或表示方法中正确的是 [???? ]
A.等质量的硫蒸气和硫磺分别完全燃烧,后者放出的热量多
B.反应热的大小与反应物的多少无关
C.已知强酸与强碱反应的中和热为57.3 kJ・mol-1,若将含0.5mol H2SO4的浓溶液与含1mol NaOH的溶液混合,放出的热量要大于57.3 kJ
D.Ba(OH)2・8H2O(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l);△H<0
参考答案:C
本题解析:
本题难度:一般
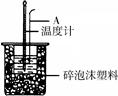
3、实验题 (16分)50mL 0.50mol/L盐酸跟50mL 0.55 mol/L NaOH溶液在右图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算反应热。
(1)烧杯间填满泡沫塑料的作用是???????????????????????????????;
(2)大烧杯上若不盖硬纸板,求得的中和热数值?????????(填“偏大”、 “偏小”、“无影响”)
(3)如下图所示,仪器A的名称是_______________;在实验过程中,如果不把温度计上的酸用水冲洗干净直接测量NaOH溶液的温度,则测得的△H?????-57.3KJ/mol(填“>”、“<”或“=”);
(4)实验中改用80mL 0.50mol/L盐酸跟100mL 0.55 mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量?????????????(填“相等、“不相等”),
所求中和热??????????????(填“相等、“不相等”) 。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会??????????;(均填“偏大”、“偏小”、“无影响”)
(6)理论上稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,写出稀硫酸和稀氢氧化钠溶液反应的中和热的热化学方程式??????????????????????????????????;
参考答案:(1)保温防止热量损失。?(2)偏小??(3)环形玻璃棒;△
本题解析:(1)在实验中应该尽可能的减少热量的损失,所以烧杯间填满泡沫塑料的作用是保温防止热量损失。
(2)大烧杯上若不盖硬纸板,则会造成热量的损失,测定结果偏低。
(3)根据仪器的结构可知,应该是是环形玻璃棒。由于酸能和氢氧化钠反应放出热量,所以造成氢氧化钠溶液的起始温度高,因此导致最终放出的热量偏少,则△H>-57.3KJ/mol。
(4)改变酸和碱的用量,反应中放出的热量会变化,但反应热是不变的,因为中和热是指酸跟碱发生中和反应生成1摩尔H2O时所放出的热量,与酸碱的用量无关。
(5)
本题难度:一般
4、选择题 在50ml 0.01mol/L H2SO4溶液加入 50ml 0.01mol/LNaOH溶液时,所得溶液呈
A.无法判断
B.碱性
C.中性
D.酸性
参考答案:D
本题解析:硫酸是二元强酸,氢氧化钠是一元强碱,在体积和浓度相同额条件下,硫酸是过量的,溶液显酸性。答案选D。
本题难度:简单
5、计算题 100mL 0.1 mol・L-1HCI与等体积0.15 mol・L-1 Ba(OH)2溶液混合,求PH值(写出过程)。
参考答案:pH=13
本题解析:考查pH的有关计算
氯化氢的物质的量是0.1L×0.1mol/L=0.01mol
氢氧化钡的物质的量是0.1L×0.15mol/L=0.015mol
所以氢氧化钡是过量的根据反应式H++OH-=H2O可知
溶液中OH-的浓度是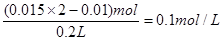
所以溶液中氢离子浓度是1×10-13mol/L因此溶液
本题难度:一般