微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 水滑石化学式为:[Mg6Al2(OH)16CO3]・4H2O(相对分子质量为602),是环保型阻燃剂。它受热时生成4种不同的氧化物,请写出该物质分解的化学方程式:?????????。
在医药上,水滑石还能作为抗酸药,作用于胃和十二指肠溃疡等,某研究型学习小组要测定一种市售的水滑石药片中水滑石的质量分数。
【查阅资料】水滑石与稀硫酸反应的化学方程式为:
[Mg6Al2(OH)16CO3]・4H2O+9H2SO4==6MgSO4+Al2(SO4)3+CO2↑+21H2O。药片中除了水滑石外含有一定量的辅料――淀粉等物质。
【提出猜想】小华想将该药片放在空气中充分灼烧完成测定;小明想通过水滑石与硫酸反应原理来完成测定,请你参与探究。
【设计方案】他们设计了不同的实验方案。
小华的方案,称取10.0g市售的水滑石药片研磨成粉末置于通风橱中,充分灼烧至质量不再减少,再称量剩余固体的质量为6.1g,减少的质量即为二氧化碳和水的总质量,则可求的水滑石药片中水滑石的质量分数为???????????%。
小明的方案:
(1)小明设计了下图所示的实验装置。取10.0g市售的水滑石药片研磨成粉末,进行实验。
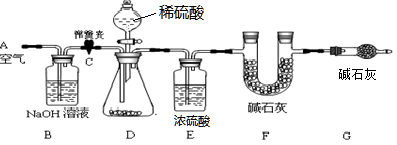
【说明】碱石灰是氧化钙和氢氧化钠固体的混合物。B装置中发生的化学方程式为?????????。
(2)操作步骤
①连接好装置,检查装置的气密性②打开弹簧夹C,在A处缓缓通入一段时间的空气③称量F的质量④关闭弹簧夹C,慢慢滴加稀盐酸至过量,直至D中无气泡冒出⑤打开弹簧夹C,再次缓缓通入一段时间空气⑥再次称量F的质量,得前后两次质量差为0.44g。
(3)问题探究
B、E装置的作用分别是????????、????????。若没有G装置,则测定的水滑石的质量分数会??????(填“偏大”、“偏小”、“不变”)。实验选用稀硫酸而不选用稀盐酸的理由是??????。
(4)数据计算
根据实验数据,可求得水滑石药片中水滑石的质量分数为????????%。(写出计算过程)
【方案评价】在上述实验方案中,你认为合理的实验方案是???????(填小华或小明),另一个方案不合理的原因是???????。
参考答案:(12分)[Mg6Al2(OH)16CO3]・4H2O
本题解析:
试题分析:根据题中所给出的反应物的组成分析,该物质分解的化学方程式是[Mg6Al2(OH)16CO3]・4H2O ??△?6MgO+Al2O3+CO2↑+12H2O↑。
根据差量法计算,固体减少的质量是CO2和12H2O的质量。
[Mg6Al2(OH)16CO3]・4H2O ??△?6MgO+Al2O3+CO2↑+12H2O↑??? ?m
602?????????????????????????????????????????????????????????????????260
m???????????????????????????????????????????????? 10.0g-6.1g=3.9g
602*3.9g=260m
解得m=9.03g
故水滑石药片中水滑石的质量分数为(9.03g/10.0g)*100%=90.3%。
(1)空气中的CO2会和NaOH溶液反应,方程式为CO2+ 2NaOH="=" Na2CO3+H2O。
(3)空气中的CO2会和NaOH溶液反应,故B装置的作用是除尽空气中的CO2,排除干扰。浓硫酸能吸收水份,故E装置的作用是除尽CO2中的水蒸气,排除干扰。G装置是防止空气中的CO2进入,故没有G装置,则测定的水滑石的质量分数会偏大。稀盐酸易挥发而稀硫酸不易挥发。
(4)设含[Mg6Al2(OH)16CO3]・4H2O质量 X
[Mg6Al2(OH)16CO3]・4H2O~CO2???????????……………………1分
602?????????????????? 44
x?????????????????? 0.44 g
602∶x =" 44" ∶0.44 g???????????……………………1分
x =60.2%?????????????????……………………1分;
小明 ;灼烧后辅料中的淀粉也会产生二氧化碳和水,导致质量分数偏大
点评:综合实验既考查知识的识记、理解、迁移、运用,又考查分析、对比、归纳等思维能力,符合素质教育培养学生能力的要求,是中考方向,对这类题目要重点训练,特别是对实验的设计和评价,更是重中之重。
本题难度:一般
2、选择题 下列实验操作正确且能达到预期目的的是
?
| 实验目的
| 操作
|
A
| 比较水和乙醇中羟基氢的活泼性强弱
| 用金属钠分别与水和乙醇反应
|
B
| 欲证明CH2=CHCHO中含有碳碳双键
| 滴入酸性KMnO4溶液,看紫红色是否褪去
|
C
| 确定碳、氯两元素非金属性的强弱
| 测定同温同浓度的Na2CO3和NaClO水溶液的pH
|
D
| 欲除去苯中混有的苯酚
| 向混合液中加入浓溴水,充分反应后,过滤
参考答案:A
本题解析:
试题分析:A、水中羟基的氢原子活泼性强于乙醇分子中羟基氢原子的活泼性,乙醇比较水和乙醇中羟基氢的活泼性强弱可以用金属钠分别与水和乙醇反应,A正确;B、丙烯醛分子中的碳碳双键和醛基均被酸性高锰酸钾溶液氧化,所以不能用滴入酸性KMnO4溶液,看紫红色是否褪去来证明CH2=CHCHO中含有碳碳双键,B不正确;C、确定碳、氯两元素非金属性的强弱,应该测定同温同浓度的Na2CO3和NaClO4水溶液的pH,C不正确;D、苯酚能与浓溴水反应,但生成的三溴苯酚又溶解在苯中,因此欲除去苯中混有的苯酚应该用氢氧化钠溶液,D不正确,答案选A。
本题难度:一般
3、实验题 碱式碳酸盐A可用作胃药,其组成可表示为Al2Mg6(OH)x(CO3)y・zH2O。某校化学兴趣小组欲测定其化学式,实验设计如下:
实验I:称取一定质量的A,加热分解至恒重。
实验Ⅱ:称取一定质量的A与足量的酸反应,测量生成CO2气体的质量。
可供选择的仪器和药品如图所示:(酸溶液限选6mol/LHCl或6mol/LH2SO4,其它试剂任选。)
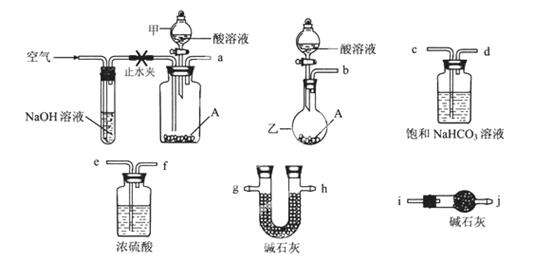
回答下列问题:
(1)仪器乙的名称为________。
(2)请选择必要的装置完成实验II,正确的连接顺序为________ (按气流方向,用接口字母表示);选用的酸溶液是________。
(3)有人提出不采用实验I,可在实验II结束后,在A完全反应后所得溶液中滴加足量的氨水,用无灰滤纸过滤,用蒸馏水洗涤反应容器2?3次,将洗涤液过滤,洗涤沉淀2?3次,将附着沉淀的滤纸放到坩埚中加热分解至恒重。判断沉淀已洗涤干净的方法是_________________,实际上未采用该方案的原因是不符合实验设计的________原则(填字母编号)。
A.科学性
B.安全性
C.可行性
D.简约性
(4)x与y的关系式是________ (用等式表示)。
(5)通过实验I的相关数据,经计算可得A的摩尔质量为602.0g. mol-1。实验II中称得样品A的质量为9.030g,与足量酸完全反应后,CO2吸收装置增重0.660g,则A 的化学式为________。
参考答案:(1)圆底烧瓶(2分) (2)a→e,f→g,h(或h,g)
本题解析:
试题分析:(1)根据仪器的结构特点可知,仪器乙的名称为圆底烧瓶。
(2)要准确测量反应中生成的CO2,则需要除去装置中残留的空气,因此反应前需要利用空气排尽装置的中的空气。由于空气中含有CO2因此空气要首先通过氢氧化钠溶液除去空气中的CO2。又因为反应中生成的CO2含有水蒸气,所以还需要先通过浓硫酸除去水蒸气,最后再通过碱石灰吸收CO2。同时为了防止空气中的CO2也被吸收,还需要再连接有个盛有碱石灰的干燥管或U形管,因此正确的连接顺序是)a→e,f→g,h(或h,g)→i。由于盐酸易挥发,所以应该选择6mol/L的硫酸。
(3)由于滤液中含有42-,因此可以通过检验42-来检验沉淀是否洗涤干净,即取少量末次沉淀洗涤液于试管中,滴加氯化钡溶液后吴浑浊,说明沉淀已洗涤干净;根据A的组成阳离子可知,生成的沉淀是氢氧化镁和氢氧化铝,但由于沉淀的生成、过滤、洗涤、干燥、称量过程过于复杂,因此实际上未采用该方案的原因是不符合实验设计的简约性,答案选D。
(4)根据化学式Al2Mg6(OH)x(CO3)y・zH2O并依据化合价代数和为0可知,x+2y=3×2+2×6=18。
(5)CO2吸收装置增重0.660g,则CO2的物质的量=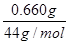 =0.015mol =0.015mol
9.030g样品的物质的量=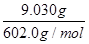 =0.015mol =0.015mol
所以根据原子守恒可知y=1
则x=18-2y=16
所以z=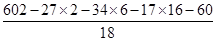 =4 =4
因此该物质的化学式为Al2Mg6(OH)16CO3・4H2O
本题难度:一般
4、实验题 课题式课堂教学是研究性学习的一种方式,其基本教学模式为

图1是关于“一氧化碳的化学性质”的课题式课堂教学中解决问题阶段,甲同学设计的证明CO具有还原性的实验装置。
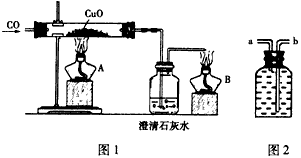
(1)实验时应先点燃______处(填“A”或“B”)的酒精灯。
(2)硬质试管中反应的化学方程式为______________________。
(3)乙同学认为甲同学设计的装置有待优化,如尾气可先储存在瓶内,然后再处理。
图2是他设计的贮气瓶,尾气应从______(选填“a”或“b”)口通入(其他装置略)
(4)丙同学质疑:CO能否使澄清石灰水变浑浊?因此,他设计在CO通入CuO之前,应先通入澄清石灰水, 以比较排除CO与澄清石灰水反应,试对此作出评价。你认为丙的设计是否有必要:_______,理由是_____________________。
(5)如果开始时通入的是CO和CO2的混合气体,则应如何设计才能达到实验目的?______________。
参考答案:(1)B
(2)CuO+CO![]() 本题解析: 本题解析:
本题难度:一般
5、选择题 某酸性溶液中可能含有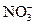 、I-、Cl-、Fe3+中的一种或几种离子,向其中加入溴水,溴水褪色,下列推测不正确的是 、I-、Cl-、Fe3+中的一种或几种离子,向其中加入溴水,溴水褪色,下列推测不正确的是
A.一定含I-
B.不含Fe3+
C.一定含Cl-
D.不含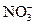
参考答案:C
本题解析:溴水褪色,一定含I-,Fe3+、NO-3(H+)不能与I-共存,一定无Fe3+、NO-3,Cl-不能确定。
本题难度:简单
|