微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知3.2?g某气体中含有3.01×1022个分子,此气体的摩尔质量是
A.32 g/mol
B.64
C.64 g/mol
D.4 g
参考答案:C
本题解析:根据n=N÷NA,所以n=3.01×1022÷6.02×1023 mol-1="0.05" mol?再由M=m÷n=3.2g÷0.05 mol=64g/mol。
本题难度:简单
2、选择题 用溶质质量分数为98%(密度为1.84 g?cm-3)的浓硫酸来配制质量分数为49%的硫酸,试确定取用的浓硫酸与水的体积比
A.小于1
B.等于1
C.大于1
D.无法确定
参考答案:A
本题解析:方法1(常规法):设浓硫酸的体积为100 mL,则其质量为100 mL×1.84 g?cm-3=184 g。根据稀释前后溶质的质量不变的原则,稀释之后溶液的质量为:184 g×98%÷49%=368 g。不难看出,需水的质量为368 g-184 g=184 g,需水的体积为184 g÷1 g?cm-3=184 mL。取用的浓硫酸与水的体积比为:100 mL∶184 mL=1∶1.84。
方法2(推理法):由于质量有加和性,所以当98%的浓硫酸与水等质量混合时,混合后的质量分数为49%,符合要求。考虑到浓硫酸密度大于水的密度,因此浓硫酸与水的体积比小于1。
本题难度:简单
3、选择题 下列有关氧气的摩尔质量表示正确的是
A.32
B.32 g
C.32 mol
D.32 g/mol
参考答案:D
本题解析:
本题难度:简单
4、选择题 2.16g? X2O5中含有0.1mol氧原子,则X的相对原子质量为
A.2.16?g
B.28
C.14
D.14g?mol-1
参考答案:C
本题解析:分析:根据X2O5含有0.1mol氧原子,则可确定X2O5的物质的量,利用M= 来计算,摩尔质量与相对分子质量在数值上相等.
来计算,摩尔质量与相对分子质量在数值上相等.
解答:X2O5中含有0.1mol氧原子,则X2O5的物质的量为0.02mol,X2O5的摩尔质量= =108g/mol,则X2O5的相对分子质量为108,则X相对原子质量=
=108g/mol,则X2O5的相对分子质量为108,则X相对原子质量= =14,
=14,
故选C.
点评:本题考查物质的量及相对分子质量的计算,熟悉摩尔质量与相对分子之间的关系即可解答,较简单.
本题难度:一般
5、选择题 某元素气态氢化物的化学式为RH3,它的最高价氧化物中含氧74%,则R的相对原子质量为
A.7
B.14
C.31
D.75
参考答案:B
本题解析:分析:元素的氢化物的化学式为RH3,则可知最高价为+5价,最高价氧化物为R2O5,根据化学式含氧量计算R的相对原子质量.
解答:元素的氢化物的化学式为RH3,则可知最高价为+5价,氧化物为R2O5,
设元素R的相对原子质量为M,则有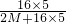 ×100%=74%,
×100%=74%,
解得M=14,
故选B.
点评:本题考查利用化学式计算相对分子质量,难度较小,注意从元素氢化物结合化合价判断最高价氧化物的化学式为解答该题的关键.
本题难度:困难