��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ��ˮ�������Ƹ����������ȵ�600��㿪ʼ�ֽ⣬�ֽ���������ƺ�����һ�ֹ��塣ijѧ������ˮ�����������Ⱥ����������ˮ�Ƴ�Ũ��Һ������ͼ��ʾ��ʵ��װ�ý���ʵ�飬����������Һ�л�������μ���ϡ���ᣬ����ʵ�������жϹ�����������ʲô�ɷ֣�

��1����������¶���600�����ϣ��������ù����������Һ�л����μ�ϡ�������������۲쵽Ʒ����Һ����ɫ��CuSO4��Һ�г��ֺ�ɫ�������Է���������Һ�п��ܳ��ֵ�����__________????????????????????_________������������������ӷ���ʽ��_____________????_??????????_��Ʒ����Һ����ɫ��ԭ���ǣ�_____________________��
��2��ͨ������ʵ�������ƶ���ˮ�����������ȷֽ�Ļ�ѧ����ʽ��____________________��װ���е�NaOH��Һ��������____________________________��
��3����������������ϡ�����Ʒ����Һ��CuSO4��Һ�ж������Ե���������ԭ����_____________________________________��
�ο��𰸣���1���е���ɫ�������ɣ���������ð�� �����������1��CuSO4��Һ�г��ֺ�ɫ������˵�������������塣Ʒ����Һ����ɫ��˵��û������SO2���������ڼ��Ⱥ������������Na2SO3��Na2S�����ʵ���֮��С��1:2����������Һ�з�Ӧ����������ֻ��H2S��������SO2����ӦʽΪSO32- + 2S2- + 6H+ ="=" 3S�� + 3H2O ��S2- + 2H+ ="=" H2S����
�����������1��CuSO4��Һ�г��ֺ�ɫ������˵�������������塣Ʒ����Һ����ɫ��˵��û������SO2���������ڼ��Ⱥ������������Na2SO3��Na2S�����ʵ���֮��С��1:2����������Һ�з�Ӧ����������ֻ��H2S��������SO2����ӦʽΪSO32- + 2S2- + 6H+ ="=" 3S�� + 3H2O ��S2- + 2H+ ="=" H2S����
��2�����������ɣ�˵���ֽⷴӦ��������ԭ��Ӧ����������һ�ֹ����������ƣ���ӦʽΪ4Na2SO3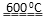 ?Na2S + 3Na2SO4�������������SO2�������ڴ�����Ⱦ���Ҫβ������������������������������H2S��SO2����ġ�
?Na2S + 3Na2SO4�������������SO2�������ڴ�����Ⱦ���Ҫβ������������������������������H2S��SO2����ġ�
��3�����ݷ�ӦSO32- + 2S2- + 6H+ ="=" 3S�� + 3H2O��֪��������Ⱥ����������Na2SO3��Na2S�����ʵ���֮�ȵ���1:2������������Һ��ǡ������S������Ʒ����Һ��CuSO4��Һ�ж������Ե�������
�����Ѷȣ�һ��
2������� ������ʵ��װ�ÿɹ�ѡ��

��ʵ�����ü״����������õ���ȩ������֤��ȩ�����ʣ���ش��������⣺
��1��Ӧѡ���װ����______����д��ţ���
��2������Ӳ�ʲ�������װ��ͭ�ۣ���д��Ӳ�ʲ������з�����Ӧ�Ļ�ѧ����ʽ______��______
��3��ʵ������۲쵽��ˮ��ɫ��Ϊ������һ����ijѧϰС���ͬѧ������ֲ��룺
A�������˼ӳɷ�Ӧ��
B��������������Ӧ��Ϊ̽�����ֲ�����ȷ��ѧϰС���ͬѧ��pH�Ʋ���ˮ��ɫǰ����Һ��pH�������Һ��pH�½�����д����ɫ�Ļ�ѧ����ʽ______
����ѡ��٢ۢ���֤��ϩ��������Ӧ�����ش��������⣺
��4��д��ʵ��������ϩ�Ļ�ѧ����ʽ______��
��5��NaOH��Һ��������______��
��6��ʵ������У����֢�����ˮ��ɫ�����û�ѧ����ʽ��ʾ��ˮ��ɫ��ԭ��______��
��7������ʲô�����˵����ϩ��������Ӧ����������______��
�ο��𰸣�I����1������ʵ��Ŀ�����ü״����������õ���ȩ��������֤��
���������
�����Ѷȣ�һ��
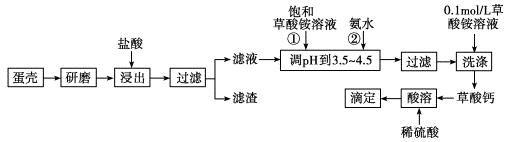
3������� ��10�֣����ǵ���Ҫ�ɷ���CaCO3�������SiO2��MgCO3��ɫ�ص����ʣ��ⶨ�����иƵĺ���ʱ���漰��ͼ�������裬�������ζ��������ñ����Ը��������Һ�ζ����ɵIJ��ᣬͨ���������Ķ�����ϵ���ɼ������Ƶĺ�����
����֧�֣��ٲ���ĵ��뷽��ʽΪH2C2O4 H����HC2O ��
�ڵζ����̵ķ�ӦΪH2C2O4��MnO ��H���D��Mn2����CO2����H2O(δ��ƽ)��
��Ksp(CaC2O4)��2.510��9��Ksp(MgC2O4)��8.610��5
�������ϲ��ϻش��������⣺
(1)��Ʒ���������õ���������Ҫ��________��
(2)�٢ڲ���ʱ�����뱥��(NH4)2C2O4��Һ�Ͱ�ˮ��������_______________��
(3)ʵ����ͨ����0.1 molL��1�������Һϴ�ӳ�������ʵ��ʱ��ˮϴ�ӳ�������ÿ��ϴ��ʱ���IJ������Һ��ˮ�������ͬ����ÿ��ϴ��ʱ�ò������Һϴ������ˮϴ����ʧ������֮��Ϊ____________��
(4)�ﵽ�ζ��յ������Ϊ��
(5)������MgCO3�Ĵ��ڣ���˷���õĸƺ�����__________ʵ��ֵ����>��=��<��
�ο��𰸣���ÿ��2�֣�
(1)SiO2
(2)���ֽϴ��C
�����������
�����Ѷȣ���
4������� ij��ȤС������ͼװ��̽�����Ĵ�����
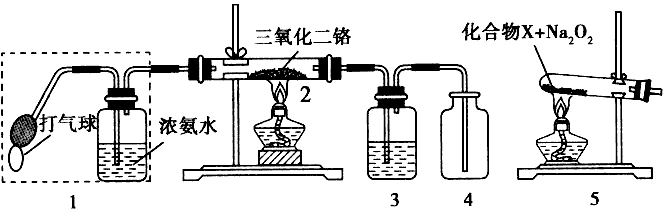
��1�����������Ļ�ѧ����ʽΪ________________��
��2�����Ȳ�����2һ��ʱ���ѹ1�д��������������۲쵽2�����ʳʺ���״̬��ֹͣ���Ⱥ����ܱ��ֺ��ȣ��÷�Ӧ��____��Ӧ������ȡ��� �ȡ�����
��3��Ϊ��֤��װ��4�й۲쵽����ɫ���壬װ��3Ӧװ��_____����ȡ��3����4 �н��۲쵽�������̣�ԭ����___________________��
��4��Ϊʵ�ְ���������Ҳ����װ��5�滻װ��____����װ�ô��ţ�����̨��X Ϊ____��ֻдһ�֣���Na2O2��������____��
�ο��𰸣���1��![]() ���������
���������
�����Ѷȣ�һ��
5��ʵ���� ij��ѧ����С��Ϊ��̽��CaCl2��Һ��Na2SO4��Һ��Ӧ��û���ȣ���������»���̣�����ɱ��пո���֪CaSO4��ˮ���ܣ�CaCO3��ˮ�����ܣ�

�ο��𰸣���Ca2++SO42-==CaSO4��
��Ӧ����
���������
�����Ѷȣ�����