微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:

提供的试剂:饱和Na2CO3溶液、?饱和K2CO3溶液?、NaOH溶液、?KOH溶液、? BaCl2溶液?、Ba(NO3)2溶液
(1)欲除去溶液中的Ca2+、Mg2+、Fe3+、SO42-离子,选出a所代表的各种试剂,按滴加顺序依次为????????????(填化学式);
(2)蒸发浓缩溶液Ⅱ得到的糊状物的化学成分最多的是(填化学式);
(3)用提纯过的NaCl固体来配制480 mL 0.4 mol・L-1NaCl溶液时,所用仪器除烧杯、药匙、玻璃棒、天平、胶头滴管外还有?(填仪器名称);需NaCl?g。
(4)电解饱和食盐水的装置如图所示:

若收集到的H2为2 L,则同样条件下收集到的Cl2体积??(填“>”、“=”或“<”)2 L,其原因是:?????????(文字描述);若将此装置的b口密封住,则电解一段时间后,U型管中可以获得一种消毒液,写出获得此消毒液的一个总反应方程式:??????????????。
参考答案:(本小题12分)
(1)滴加顺序为:?B
本题解析:略
本题难度:一般
2、简答题 (16分)某同学从网络上了解到菠菜中富含可溶性的两类正盐:草酸盐和碳酸盐。该同学欲用实验验证这一事实并检测其中草酸盐的含量。查阅资料得知草酸(H2C2O4)是一种二元有机弱酸,具有较强的还原性;草酸钙(CaC2O4)不溶于水能溶于稀硫酸。请回答下列问题:
(1)该学生将菠菜研磨成粉末、热水浸泡、过滤得到澄清溶液A。研磨菠菜使用的实验仪器的名称为????????????。
(2)设计实验方案验证菠菜中含有草酸盐和碳酸盐,补充完成预期现象和结论。
实验步骤
| 预期现象和结论
|
步骤1:调节溶液A至弱碱性,滴加足量CaCl2溶液。
| ①出现白色沉淀,说明菠菜中?????
?????????????????????????。
|
步骤2:取步骤1的沉淀于试管中,加入足量的稀硫酸,沉淀完全溶解,并将产生的无色无味的气体通入澄清石灰水中。
| ②????????????????????????。
|
步骤3:向步骤2得到的溶液中滴加几滴高锰酸钾溶液。
| ③????????????????????????。
(3)欲准确测定菠菜中草酸盐的含量
①操作:取m g菠菜样品,将其中草酸盐全部转化为CaC2O4沉淀分离出来置于烧杯中,用过量的稀硫酸完全溶解后,溶液转入?????中并加水配制成250mL溶液。每次移取25.00mL该溶液于锥形瓶中,用0.0100mol・L-1 KMnO4标准溶液滴定,平均消耗标准溶液V mL。KMnO4滴定实验时发生的离子方程式为????。
②计算:菠菜中草酸盐(以C2O42-计算)的质量分数为(可以只列式不化简)??????。
③误差分析: 下列操作会使测定结果偏高的是???????。
A.配制溶液时未洗涤烧杯和玻璃棒就加水定容
B.锥形瓶未干燥就加入待测液进行滴定
C.未用标准液润洗就加入标准液开始滴定
D.滴定前尖嘴处有气泡滴定后气泡消失
E.滴定后俯视读数
参考答案:(1)研钵(2分)。
(2)①至少含有C2O42-、C
本题解析:
试题分析:(1)固体研磨用到的仪器为研钵,研磨菠菜使用的实验仪器的名称为研钵。(2)草酸钙和碳酸钙均为不溶于水的白色固体,步骤1中出现白色沉淀,说明菠菜中至少含有C2O42-、CO32-中的一种或两种皆有;步骤2的目的是验证菠菜中含有碳酸盐,选用稀盐酸溶解沉淀,方法是:加入足量1 mol?L-1?HCl,将产生的气体通入足量澄清石灰水中,现象是沉淀溶解,澄清石灰水变浑浊,说明菠菜中含有碳酸盐;步骤3操作目的是验证草酸盐的存在,利用草酸盐具有还原性,方法是;向步骤2得到的溶液中滴加几滴0.01 mol?L-1?KMnO4,现象是溶液紫红色褪去,说明菠菜中含有草酸盐,答案是①至少含有C2O42-、CO32-中的一种或两种皆有。②澄清石灰水变浑浊,说有菠菜中含有CO32-。③高锰酸钾紫色褪去,说明菠菜中含有C2O42-。(3)①配制250mL溶液应选用250mL容量瓶;KMnO4标准溶液与C2O42-反应生成+2价锰离子、二氧化碳和水,离子方程式为2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O。②计算:根据反应方程式得关系式:5C2O42-――2KMnO4,代入题给数据计算,菠菜中草酸盐(以C2O42-计算)的质量分数为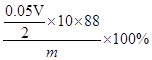 ×10-3。③误差分析: A.配制溶液时未洗涤烧杯和玻璃棒就加水定容,高锰酸钾溶液的体积偏小,测定结果偏低,错误,B.锥形瓶未干燥就加入待测液进行滴定,对测定结果无影响,错误;C.未用标准液润洗就加入标准液开始滴定,高锰酸钾溶液的体积偏大,测定结果偏高,正确;D.滴定前尖嘴处有气泡滴定后气泡消失,高锰酸钾溶液的体积偏大,测定结果偏高,正确;E.滴定后俯视读数,高锰酸钾溶液的体积偏小,测定结果偏低,错误,选CD。 ×10-3。③误差分析: A.配制溶液时未洗涤烧杯和玻璃棒就加水定容,高锰酸钾溶液的体积偏小,测定结果偏低,错误,B.锥形瓶未干燥就加入待测液进行滴定,对测定结果无影响,错误;C.未用标准液润洗就加入标准液开始滴定,高锰酸钾溶液的体积偏大,测定结果偏高,正确;D.滴定前尖嘴处有气泡滴定后气泡消失,高锰酸钾溶液的体积偏大,测定结果偏高,正确;E.滴定后俯视读数,高锰酸钾溶液的体积偏小,测定结果偏低,错误,选CD。
本题难度:简单
3、选择题 现有三组溶液:①汽油和氯化钠溶液?②39%的乙醇溶液?③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
A.分液、萃取、蒸馏
B.萃取、蒸馏、分液
C.分液、蒸馏、萃取
D.蒸馏、萃取、分液
参考答案:C
本题解析:
试题分析:萃取适合于溶质在不同溶剂中的溶解性不同而分离的一种方法,分液适用于互不相溶的液体之间的一种分离方法,蒸馏是依据混合物中个组分沸点不同而分离的一种法,适用于除去易挥发、难挥发或不挥发杂质,据此解答。汽油不溶于水,分液即可;乙醇与水互溶,与水的沸点相差较大,可以蒸馏进行分离;单质溴易溶在有机溶剂中,萃取即可,因此正确的答案选C。
本题难度:一般
4、选择题 除去下列物质中所含的少量杂质,下表中除杂方法正确的是
选项
| 物?质
| 所含杂质
| 除杂质的方法
| A
| 氧化铜
| 氯化钠
| 加水溶解、过滤、蒸发结晶
| B
| 氧气
| 水蒸气
| 通过盛有浓硫酸的洗气瓶
| C
| 硫酸钠溶液
| 稀硫酸
| 加入过量碳酸钠溶液,过滤
| D
| 二氧化碳
| 一氧化碳
| 点燃
参考答案:B
本题解析:
试题分析:A项:只用溶解、过滤就行了,故错;C、D项:引入新的杂质,故错。故选B。
点评:除杂一般有两种方法,将杂质彻底除去或将杂质转化为主物质,所选物质不能与主物质发生反应,也不要在除去杂质的同时又混入了其它物质。
本题难度:简单
5、选择题 下列物质中,分子物质的量最多的是(相对原子质量??H-1??O-16)
A.1molN2
B.1g?H2
C.0.1NAO2
D.4℃时,20mL水
参考答案:D
本题解析:分析:A、N2物质的量为1mol;
B、用质量和摩尔质量物质换算出物质的量;
C、用微粒数目和阿伏伽德罗常换算出物质的量;
D、用密度和体积计算质量,再用质量和摩尔质量物质换算出物质的量.
解答:A、N2物质的量为1mol;
B、1g?H2物质的量为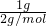 =0.5mol; =0.5mol;
C、0.1NAO2的物质的量为: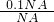 =0.1mol; =0.1mol;
D、4℃时,20mL水的物质的量为: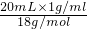 =1.11mol; =1.11mol;
故选D.
点评:本题考查了物质的量与质量、微粒数目的换算关系和计算,同时还考查了质量、密度和体积的关系,较简单.
本题难度:简单
|
|