微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是( ? )
A.含有共价键的化合物一定是共价化合物
B.在气态单质分子中,一定存在共价键
C.在共价化合物中,一定存在着共价键
D.只含离子键的化合物才是离子化合物
参考答案:C
本题解析:
本题难度:简单
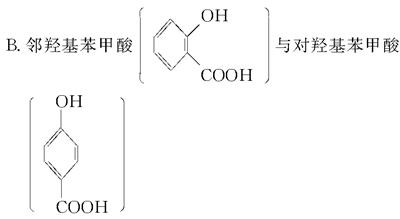
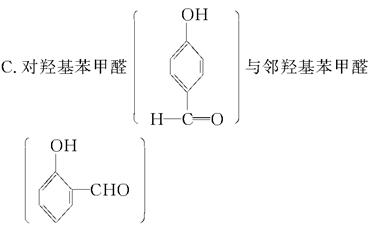
2、选择题 下列化合物的沸点相比较,前者低于后者的是(??)。
A.乙醇与氯乙烷
 ?
?
D.H2O与H2Te
参考答案:B
本题解析:B项:前者形成分子内氢键,后者形成分子间氢键,所以后者沸点高。
本题难度:一般
3、选择题 与Ne核外电子排布相同的离子跟与Ar核外电子排布相同的离子形成的化合物是[???? ]
A.MgBr2
B.Na2S
C.KCl
D.HF
参考答案:B
本题解析:
本题难度:简单
4、填空题 (1)写出CO2+离子基态的价电子排布式:__________________________________。
(2)SO32-的空间构型是:___________________________________________。
(3)OCN-与CO2是等电子体,则OCN-中C原子的杂化方式是:_______________。
(4)六方氮化硼(BN)晶体具有很高的熔点,B原子和N原子均为sp2杂化。该晶体中存在的作用力有:__________________。
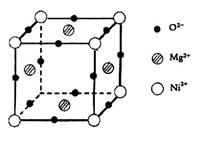
(5)元素O、Mg、Ni可形成一种晶体,其晶胞如图所示。在晶体中,每个Ni2+离子与_____________个Mg2+离子配位。该晶体的化学式是____________。
参考答案:(1)3d7(1分)?(2)三角锥形(1分)?(3)sp(1
本题解析:
试题分析:(1)Co原子序数为27,Co2+失去了2个电子,价电子排布式为3d7
(2)根据价电子互斥理论可推出SO32-的空间构型是三角锥形。
(3)等电子体结构相似,所以OCN-中C原子的杂化方式与CO2相同。
(4)N、B之间形成共价键,六方氮化硼(BN)晶体为层状结构,层与层之间作用力为范德华力。
(5)根据晶胞的结构,结合立体几何知识可看出每个Ni2+离子与8个Mg2+离子配位;该晶胞含O2?:12×1/4="3," Mg2+: 4×1/2="2" , Ni2+:
本题难度:一般
5、选择题 下列说法错误的是( )
A.全部由非金属元素组成的化合物可能是离子化合物
B.在共价化合物中一定含有共价键
C.含有离子键的化合物一定是离子化合物
D.含有共价键的化合物一定是共价化合物
参考答案:D
本题解析:
本题难度:简单