微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列对分子结构叙述正确的是???????????????????????????????????????????????(???)
A.H2O2分子中,两个O之间形成2对共用电子对
B.N2的电子式是N┇┇N
C.CO2和CS2都是直线型分子
D.白磷和甲烷都是正四面体型,键角都是109°28′
参考答案:C
本题解析:
试题分析:.H2O2分子中,两个O之间形成1对共用电子对,A不正确。B不正确,氮气的电子式是 。D不正确,白磷的键角是60°,答案选C。
。D不正确,白磷的键角是60°,答案选C。
点评:该题是高考中的常见考点和题型,属于中等难度题的考查。试题综合性强,难易适中,在注重对学生基础知识巩固和训练的同时,侧重对学生能力的培养和训练,有利于培养学生
本题难度:简单
2、选择题 石墨晶体中不存在的化学作用力是( )
A.共价键
B.氢键
C.金属键
D.范德华力
参考答案:B
本题解析:石墨是一种混合型晶体。石墨晶体中,同一层里面的碳原子之间以共价键相互结合,层与层之间是范德华力,石墨中的碳原子采取的是sp2杂化,每一个碳原上都有一个2p轨道与平面垂直,p电子可以在同一层中自由移动。只有氢键不存在,所以应该选择B项。
本题难度:简单
3、选择题 在下列有关晶体的叙述中正确的是
A.晶体中有阳离子就一定存在阴离子
B.分子晶体中一定存在共价键和分子间作用力
C.金属晶体的熔点一定比分子晶体高
D.原子晶体中,一定只存在共价键
参考答案:D
本题解析:
试题分析:A.在金属晶体中有阳离子但是没有阴离子存在。错误。B.在分子晶体中一定存在分子间作用力,但是不一定存在共价键。如惰性气体就是单原子分子,没有化学键存在。错误。C.一般情况下金属晶体的熔点比分子晶体高,但是也有例外。如Hg在常温下是液体,而S单质为分子晶体,熔点S>Hg。错误。D.在原子晶体中,原子间以共价键结合形成空间网状结构,断裂较难,因此熔沸点高,硬度大,难溶于一般的溶剂。正确。
本题难度:一般
4、判断题 试从不同角度解释:乙醇(C2H5OH)和二甲醚(CH3OCH3)的化学组成均为C2H6O,但乙醇的沸点为78.5℃,而二甲醚的沸点为-23℃?
参考答案:①乙醇的极性强,分子间作用力大,沸腾时需要提供更多的能量去破
本题解析:
乙醇(C2H5OH)和二甲醚(CH3OCH3)的化学组成相同,两者的相对分子质量也相同,不同的是二者的极性、对称性不同,且乙醇能满足氢键的形成条件,从不同点加以解释。
本题难度:一般
5、选择题 在某晶体中,与某一个微粒x距离最近且等距离的另一个微粒y所围成的空间构型为正八面体形(如图)。该晶体不是( )
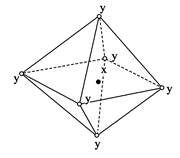
A.NaCl(x=Na+,y=Cl-)
B.CsCl(x=Cs+,y=Cl-)
C.金属钋(Po)
D.MgO晶体
参考答案:B
本题解析:
试题分析:根据题干分析,与x最近且距离相等的有6个y,说明不是CsCl,氯化铯中应该是与x最近且距离相等的有8个y。
点评:属于较简单题。
本题难度:一般