微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
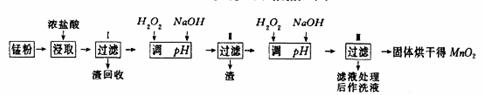
填空题 (16分)回收的废旧锌锰干电池经过处理后可得到锰粉(主要含MnO2、Mn(OH)2、Fe、NH4Cl和炭黑等),由锰粉制取MnO2的步骤和数据如下:
物质
| 开始沉淀
| 沉淀完全
|
Fe(OH)3
| 2.7
| 3.7
|
Fe(OH)2
| 7.6
| 9.6
|
Fe(OH)2
| 8.3
| 9.8
??(1)在加热条件下,用浓盐酸浸取锰粉得到含有Mn2+、Fe3+等离子的溶液,MnO2与浓盐酸反应的离子方程式?????????,该处理方法的缺点?????????。
(2)步骤I中滤渣的化学式???来源:91考试 网??????,步骤I中滤渣的化学式?????????。
(3)向步骤I的滤液中加足量H2O2的作用为?????????。再加NaOH溶液调节pH在3.7<pH<8.3,目的是???????????????????。
(4)向步骤II的滤液中H2O2溶液,再加NaOH溶液调节pH为9,使Mn2+转化成MnO2,在这一过程中H2O2起?????????(填氧化剂、还原剂)的作用。
填空题 (16分)回收的废旧锌锰干电池经过处理后可得到锰粉(主要含MnO2、Mn(OH)2、Fe、NH4Cl和炭黑等),由锰粉制取MnO2的步骤和数据如下:

物质
| 开始沉淀
| 沉淀完全
| Fe(OH)3
| 2.7
| 3.7
| Fe(OH)2
| 7.6
| 9.6
| Fe(OH)2
| 8.3
| 9.8
??(1)在加热条件下,用浓盐酸浸取锰粉得到含有Mn2+、Fe3+等离子的溶液,MnO2与浓盐酸反应的离子方程式?????????,该处理方法的缺点?????????。
(2)步骤I中滤渣的化学式?????????,步骤I中滤渣的化学式?????????。
(3)向步骤I的滤液中加足量H2O2的作用为?????????。再加NaOH溶液调节pH在3.7<pH<8.3,目的是???????????????????。
(4)向步骤II的滤液中H2O2溶液,再加NaOH溶液调节pH为9, 使Mn2+转化成MnO2,在这一过程中H2O2起?????????(填氧化剂、还原剂)的作用。
本题答案:
(1)MnO2+4H++2Cl-![]() 本题解析:略 本题解析:略
本题所属考点:【气体的净化、干燥、吸收与收集】
本题难易程度:【简单】
He who is first come is first served. 先到的先得。 |
|