微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
实验题 用2.4 mol/L的H2SO4溶液配制100mL浓度为0.2 mol/L的稀H2SO4,回答下列问题:
(1)需用量筒量取2.4 mol/L的H2SO4溶液的体积是?????????mL。
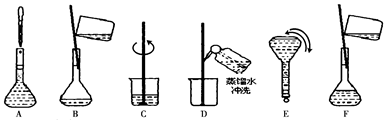
(2)溶液配制的所需的基本步骤如下:
将上述实验步骤A到F按实验过程先后次序排列___________________?????????。
(3)上述实验步骤A、B、E、F都用到的仪器名称为___ _______。??
(4)取上述所配溶液10mL与足量BaCl2溶液反应,生成白色沉淀0.48 g。则该溶液
浓度???????0.2 mol/L(填“大于”“等于”或“小于”),造成此误差的操作可能
是??????。?
a. 定容时俯视容量瓶;? b. 用量筒取2.4 mol/LH2SO4溶液时俯视读数;
c. 容量瓶使用前未干燥;d. 使用的烧杯和玻璃棒未洗涤彻底;
e. 定容时将蒸馏水洒在容量瓶外面
实验题 用2.4 mol/L的H2SO4溶液配制100mL浓度为0.2 mol/L的稀H2SO4,回答下列问题:

(1)需用量筒量取2.4 mol/L的H2SO4溶液的体积是?????????mL。
(2)溶液配制的所需的基本步骤如下:
将上述实验步骤A到F按实验过程先后次序排列___________________?????????。
(3)上述实验步骤A、B、E、F都用到的仪器名称为__________。??
(4)取上述所配溶液10mL与足量BaCl2溶液反应,生成白色沉淀0.48 g。则该溶液
浓度???????0.2 mol/L(填“大于”“等于”或“小于”),造成此误差的操作可能
是??????。?
a. 定容时俯视容量瓶;? b. 用量筒取2.4 mol/LH2SO4溶液时俯视读数;
c. 容量瓶使用前未干燥;d. 使用的烧杯和玻璃棒未洗涤彻底;
e. 定容时将蒸馏水洒在容量瓶外面
本题答案:(8分)(1)8.3(2分)
(2)CBDFAE;(2
本题解析:
试题分析:(1)根据稀释定律,稀释前后溶质硫酸的物质的量不变,设浓硫酸的体积为xmL,所以xmL×2.4mol/L=100mL×0.2mol/L,解得:x≈8.3,所以应量取的硫酸体积是8.3mL;故答案为:8.3mL。
(2)配制步骤有量取、稀释、移液、洗涤、定容、摇匀等操作,用10mL量筒量取(用到胶头滴管)硫酸,在烧杯中稀释,并用玻璃棒搅拌,冷却后转移到100mL容量瓶中,并用玻璃棒引流,洗涤烧杯与玻璃棒2~3次,并移入容量瓶内,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,盖好瓶塞,反复颠倒摇匀,故操作顺序为CBDFAE。
(3)从图中观察得到,A、B、E、F都用到的仪器名称为100mL容量瓶。
(4)白色沉淀是硫酸钡,硫酸钡的物质的量为0.48g÷233g/mol="0.48/233" mol,所以n(H2SO4)=n(BaSO4)="=0.48/233" mol ,故所配硫酸溶液的浓度为0.48/233 mol÷0.01L=0.21mol/L>0.2mol/L;
a.定容时俯视容量瓶,所配溶液体积偏小,配制人一样的浓度偏大,故a符合;
b.用量筒取2.4mol/LH2SO4溶液时俯视读数,量取硫酸溶液的体积偏小,所配溶液的浓度偏小,故b不符合;
c.配制需加水定容,使用容量瓶前未干燥,对所配溶液浓度无影响,故c不符合;
d.使用的烧杯和玻璃棒未洗涤彻底,移入容量瓶内溶质硫酸的物质的量偏小,所配溶液浓度偏小,故d不符合;
e.定容时将蒸馏水洒在容量瓶外面,可以继续加水,对所配溶液浓度无影响,故e不符合;
故答案为:大于,A.
点评:本题考查了一定物质的量浓度溶液的配制,难度不大,注意从c= n/V理解溶液配制与误差分析。
本题所属考点:【气体的净化、干燥、吸收与收集】
本题难易程度:【简单】
He who knows nothing but pretends to know everything,is indeed a good-for-nothing. 不懂装懂,永世饭桶.