微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
实验题 某化学实验小组为验证常见还原剂SO2、I-、Fe2+的还原性强弱的顺序为:
SO2>I->Fe2+,用下图所示装置进行实验(加热和夹持装置已略,气密性已检验)。
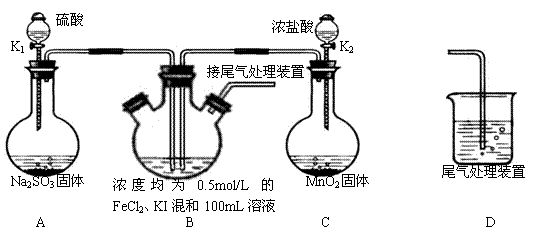
(1)上述实验需要加热的装置是
(2)D中,烧杯盛放的是
(3)实验开始时,关闭K1,打开K2,通入少量氯气,写出B中发生反应的离子方程式 ________________
①为验证I-的还原性比Fe2+ 强,取(3)后B中的少量溶液于试管中,应再往试管中滴入 ________ 溶液,现象是
②在(3)后,为了比较SO2和I-的还原性强弱,接下来的操作是
A.关闭K2开K1
B.关闭K1打开K2
C.同时打开K1和K2
(4)若打开K2,通入Cl2恰好将Fe2+、I-全部氧化后,再打开K1通入SO2,当Fe3+全部转化为Fe2+时,此时通入的SO2的体积(标准状况下)为 ??________??
实验题 某化学实验小组为验证常见还原剂SO2、I-、Fe2+的还原性强弱的顺序为:
SO2>I->Fe2+,用下图所示装置进行实验(加热和夹持装置已略,气密性已检验)。

(1)上述实验需要加热的装置是
(2)D中,烧杯盛放的是
(3)实验开始时,关闭K1,打开K2,通入少量氯气,写出B中发生反应的离子方程式 ________________
①为验证I-的还原性比Fe2+强,取(3)后B中的少量溶液于试管中,应再往试管中滴入 ________ 溶液,现象是
②在(3)后,为了比较SO2和I-的还原性强弱,接下来的操作是
A.关闭K2开K1
B.关闭K1打开K2
C.同时打开K1和K2
(4)若打开K2,通入Cl2恰好将Fe2+、I-全部氧化后,再打开K1通入SO2,当Fe3+全部转化为Fe2+时,此时通入的SO2的体积(标准状况下)为 ??________??
本题答案:(13分 除第一空一分外其余每空二分)(1)C?(2)NaO
本题解析:
试题分析:(1)实验室制备氯气需要加热,则需要加热的装置是C装置,答案选C。
(2)由于SO2和氯气都是大气污染物,需要尾气处理,所以D中烧杯盛放的氢氧化钠溶液。
(3)①由于碘离子的还原性强于亚铁离子,则氯气首先氧化的是碘离子,反应的离子方程式是2I-+ Cl2 =I2 + 2Cl- 。检验单质碘碘生成可以用淀粉溶液,实验现象是溶液呈蓝色。
②要比较SO2和I-的还原性强弱,则需要通过A装置制备SO2,所以正确的操作是关闭K2开K1,答案选A。
(4)碘离子和亚铁离子碘物质的量均是0.1L×0.5mol/L=0.05mol,通入SO2后,SO2分别将铁离子和单质碘还原为亚铁离子和碘离子,但由于铁离子的氧化性强于单质碘的,所以当Fe3+全部转化为Fe2+时,根据电子得失守恒可知,需要SO2的物质的量是0.05mol÷2=0.025mol,在标准状况下的体积是0.025mol×22.4L/mol=0.56L。2的制备、氧化还原反应的有关判断和计算、化学实验基本操作
点评:本题高考中的常见题型,属于中等难度的试题。试题基础性强,贴近高考,在注重对学生基础知识巩固和训练对同时,侧重对学生能力的培养,有利于培养学生规范严谨的实验设计能力和动手操作能力,也有助于提升学生的学科素养 。
本题所属考点:【气体的净化、干燥、吸收与收集】
本题难易程度:【一般】
A baited cat may grow as fierce as a lion. 被逼急的猫,凶得象狮子。