微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
实验题 (14分)曾经有一种固氮的方法:1100°C通N2和CaC2反应得到CaCN2 。
已知:CaCN2+3H2O = 2NH3+CaCO3;CaC2+2H2O = C2H2↑+Ca(OH)2
 ?
?
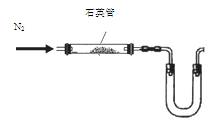
(1)某同学采用以下装置(加热和夹持仪器已略去)制取少量的CaCN2
①U形管中盛放的物质是?????????(填一种);
②???(填“能”或“不能”)用普通玻璃管代替图中石英管;
(2)检验反应后的固体(用W表示)中含有氮元素该同学将适量W溶于水,有气泡产生,说明固体中含有氮元素,该结论不正确。若要得出正确结论,还需进行的实验是?????????????????????? 。
(3)测定W中CaCN2的质量分数
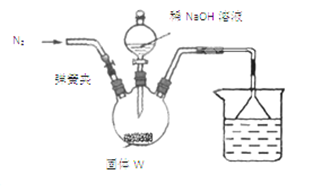
步骤Ⅰ:按如图所示装置(夹持仪器已略去)进行实验:关闭弹簧夹,将漏斗中溶液逐滴加入到三颈瓶中,当W反应完全后,打开弹簧夹,通入氮气,直至氨气被200mL0.1 mol・L-1硫酸完全吸收。
步骤Ⅱ:准确量取烧杯中溶液20.00mL置于锥形瓶中,滴入几滴指示剂,用cmol・L-1NaOH溶液滴定过量的硫酸,实验测得消耗标准溶液的平均体积为vmL。
已知三种常用指示剂变色pH范围如下:
指示剂
| a
| b
| c
|
变色pH范围
| 3.1~4.4
| 8.0~10.0
| 4.4~6.2
|
说明
| pH<3.1显红色
pH>4.4显黄色
| pH<8.0显无色
pH>10.0显红色
| pH<4.4显红色
pH>6.2显黄色
①上述滴定过程中,不宜选用的指示剂是?????????????????(填字母序号);
②烧杯中最终吸收氨气的物质的量为??????????mol;经进一步计算可求得W中CaCN2质量分数。
③上述实验所得结果明显偏小,若不考虑装置的气密性和操作误差,则导致结果偏小的可能原因是??
????????????????(写1种)。
实验题 (14分)曾经有一种固氮的方法:1100°C通N2和CaC2反应得到CaCN2 。
已知:CaCN2+3H2O = 2NH3+CaCO3;CaC2+2H2O = C2H2↑+Ca(OH)2
 ? ?
(1)某同学采用以下装置(加热和夹持仪器已略去)制取少量的CaCN2
①U形管中盛放的物质是?????????(填一种);
②???(填“能”或“不能”)用普通玻璃管代替图中石英管;
(2)检验反应后的固体(用W表示)中含有氮元素该同学将适量W溶于水,有气泡产生,说明固体中含有氮元素,该结论不正确。若要得出正确结论,还需进行的实验是??????????????????????。
(3)测定W中CaCN2的质量分数
步骤Ⅰ:按如图所示装置(夹持仪器已略去)进行实验:关闭弹簧夹,将漏斗中溶液逐滴加入到三颈瓶中,当W反应完全后,打开弹簧夹,通入氮气,直至氨气被200mL0.1 mol・L-1硫酸完全吸收。
步骤Ⅱ:准确量取烧杯中溶液20.00mL置于锥形瓶中,滴入几滴指示剂,用cmol・L-1NaOH溶液滴定过量的硫酸,实验测得消耗标准溶液的平均体积为vmL。
已知三种常用指示剂变色pH范围如下:
指示剂
| a
| b
| c
| 变色pH范围
| 3.1~4.4
| 8.0~10.0
| 4.4~6.2
| 说明
| pH<3.1显红色
pH>4.4显黄色
| pH<8.0显无色
pH>10.0显红色
| pH<4.4显红色
pH>6.2显黄色
①上述滴定过程中,不宜选用的指示剂是?????????????????(填字母序号);
②烧杯中最终吸收氨气的物质的量为??????????mol;经进一步计算可求得W中CaCN2质量分数。
③上述实验所得结果明显偏小,若不考虑装置的气密性和操作误差,则导致结果偏小的可能原因是??
????????????????(写1种)。
本题答案:(1)①碱石灰或无水氯化钙等???(2分)②不能??(2分)
本题解析:
试题分析:(1)①由于碳化钙极易与水反应,因此U形管中有关盛放固体干燥剂防止水蒸气进入,因此可以是碱石灰或无水氯化钙等。
②由于普通玻璃中含有二氧化硅,而在高温下二氧化硅能与碳酸钙反应生成硅酸钙和CO2,所以不能用普通玻璃管代替图中石英管。
(2)由于过量的碳化钙也能与水反应产生气泡,因此要验证含有氮元素,还必须检验生成的气体中含有氨气,所以正确的操作是将湿润的红色石蕊试纸置于容器口,试纸变蓝色,说明 91EXAm.org固体中含有氮元素。
(3)①滴定前溶液显酸性,而b指示剂在酸性条件下是无色的,当硫酸恰好被反应后,硫酸铵溶液还是显酸性的,因此如果用b指示剂,溶液仍然是无色的,因此不宜选用的是b。
②消耗氢氧化钠的物质的量是0.001cvmol,则根据反应式2NaOH+H2SO4=Na2SO4+2H2O可知剩余硫酸的物质的量是0.0005cvmol×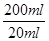 ?=0.005cvmol,所以与氨气反应的硫酸的物质的量是0.02mol-0.005cvmol,则与硫酸反应的氨气的物质的量是(0.02mol-0.005cvmol)×2=(0.04-0.01cv)mol。 ?=0.005cvmol,所以与氨气反应的硫酸的物质的量是0.02mol-0.005cvmol,则与硫酸反应的氨气的物质的量是(0.02mol-0.005cvmol)×2=(0.04-0.01cv)mol。
③由于反应需要加热且反应中有碳酸钙生成,因此如果实验所得结果明显偏小,则可能的原因是步骤Ⅰ中未加热反应容器或生成碳酸钙覆盖在固体表面,导致反应不完全。
本题所属考点:【气体的净化、干燥、吸收与收集】
本题难易程度:【一般】
Every man is best known to himself. 自己最了解自己./知已莫若已. |
|