微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在稀硫酸中加入铜粉,铜粉不溶解,再加入下列固体粉末:①FeCl2;②Fe2O3;③Zn;④KNO3,铜粉可溶解的是[???? ]
A.①②
B.②④
C.②③
D.①④
参考答案:B
本题解析:
本题难度:简单
2、选择题 将铁屑溶于过量盐酸后,再加入下列物质,不会有三价铁生成的是
[???? ]
A.硫酸
B.氯水
C.硝酸锌
D.溴水
参考答案:A
本题解析:
本题难度:简单
3、简答题 氯化铁能腐蚀铜(2FeCl3+Cu=2FeCl2+CuCl2),工业上常用此原理生产印刷线路板(步骤Ⅰ).从废液中回收铜并得到FeCl3溶液循环利用的主要流程如下:
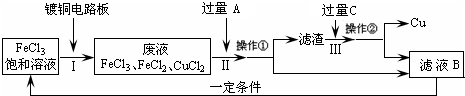
(1)写出步骤Ⅱ中发生反应的离子方程式______.
(2)试剂C是(填名称)______.
(3)若在实验室中完成上述流程,操作①中属于______操作(填名称).
(4)在步骤Ⅲ中加入过量C溶液的目的是______.
参考答案:(1)步骤Ⅱ是加入过量铁和氯化铁、氯化铜反应,最终得到氯化亚
本题解析:
本题难度:一般
4、填空题 (I)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板.用FeCl3溶液做腐蚀液与Cu反应生成CuCl2和FeCl2.
(1)写出该反应的化学方程式______.
(2)检验溶液中Fe3+存在的试剂是______,证明Fe3+存在的现象是______.
(Ⅱ)印刷电路的废腐蚀液含有大量CuCl2、FeCl2、FeCl3,任意排放会造成环境污染及资源的浪费.通过下列流程可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用.

(1)步骤①中发生反应的离子方程式______.
(2)步骤②需加入的试剂A是______(填化学式).
(3)步骤③通入的气体B是______(填化学式),写出该反应的化学方程式______.
(4)为测定滤渣中铜的质量分数,取50g的滤渣与足量的试剂A反应,得到5.6L气体(标准状况下),试计算滤渣中铜的质量分数.(写出计算过程)
参考答案:(I)(1)氯化铁与铜反应生成氯化亚铁与氯化铁,反应方程式为
本题解析:
本题难度:一般
5、选择题 某溶液中滴入KSCN溶液后变红,说明该溶液中存在[???? ]
A.Al3+ ???
B.Fe3+ ????????
C.Fe2+ ???????
D.Cu2+
参考答案:B
本题解析:
本题难度:简单