微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 自然界中已发现的100多种元素里,金属元素约占??????,其中含量最多的元素是??????,含量最多的金属元素是??????。金属导电靠??????,电解质溶液导电靠?????,金属导电能力随温度升高而???????,溶液导电能力随温度升高而???????。
参考答案: 本题解析:金属导电是由于金属晶体中存在自由移动的电子,而电解质溶液的导电是溶液中的阴、阳离子在外加电场的作用下做定向移动。温度升高时,金属晶体内部的金属阳离子运动速度加快,使电子的传递受影响,导电性减弱。温度升高时,电解质溶液中的自由移动的离子运动速率加快,导电性增强。
本题解析:金属导电是由于金属晶体中存在自由移动的电子,而电解质溶液的导电是溶液中的阴、阳离子在外加电场的作用下做定向移动。温度升高时,金属晶体内部的金属阳离子运动速度加快,使电子的传递受影响,导电性减弱。温度升高时,电解质溶液中的自由移动的离子运动速率加快,导电性增强。
本题难度:简单
2、填空题 (12分)镍(Ni)可形成多种配合物,且各种配合物有广泛的用途。
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于____________晶体;基态Ni原子的电子排布式为_______________;
写出两种与配体CO互为等电子体微粒的化学式_____________、________________ 。
(2)某镍配合 物结构如图所示,分子内含有的作用力有____________(填序号)。
物结构如图所示,分子内含有的作用力有____________(填序号)。
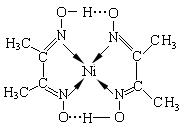
A.氢键
B.离子键
C.共价键
D.金属键 E.配位键
(3)很多不饱和有机物在Ni催化下可与H2发生加成反应,
如①CH2=CH2、②HC ≡ CH、③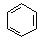 ④HCHO等,其中碳原子采取sp2杂化的分子有_________(填序号);HCHO分子的空间构型为:__________。
④HCHO等,其中碳原子采取sp2杂化的分子有_________(填序号);HCHO分子的空间构型为:__________。
(4)据报道,某种含有镁、镍和碳三种元素的晶体具有超导性,其结构如图所示。则该晶体的化学式为__________ 。晶体中每个镁原子周围距离最近的镍原子有_________个。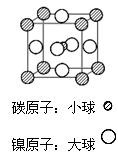
参考答案:(12分)
(1)分子(1分)
1s22s22p
本题解析:略
本题难度:一般
3、简答题 硼(B)、铝(Al)、镓(Ga)均属于硼族元素(第ⅢA族),它们的化合物或单质
都有重要用途。回答下列问题:
(1)写出基态镓原子的电子排布式?????????????。
(2)已知:无水氯化铝在178℃升华,它的蒸气是缔合的双分于(Al2Cl6),更
高温度下Al2Cl6则离解生成A1Cl3单分子。
①固体氯化铝的晶体类型是??????????????;
②写出Al2Cl6分子的结构式???????????????;
 ③单分子A1Cl3的立体构型是???????????,缔合双分子Al2Cl6中Al原子的轨道杂化类型是???????????。
③单分子A1Cl3的立体构型是???????????,缔合双分子Al2Cl6中Al原子的轨道杂化类型是???????????。
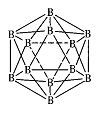
(3)晶体硼的结构单元是正二十面体,每个单元中有12个硼原予(如图)
其中有两个原子为10 B,其余为11B,则该结构单元有???种不同的结构
类型。
(4)金属铝属立方晶系,其晶胞边长为405 pm,密度是2.70g・cm-3,计算确
定其晶胞的类型(简单、体心或面心立方)???????;晶胞中距离最近的铝原
子可看作是接触的,列式计算铝的原子半径r(A1)= ???????????????????pm。
参考答案:(1)1s2 2s22p6 3s2 3p6 3d10 4s2
本题解析:(1)镓是31号元素,其原子核外有31个电子,根据构造原理知其核外电子排
布式1s2 2s22p6 3s2 3p6 3d10 4s2 4p1?或〔Ar〕3d10 4s2 4p1?
(2)①分子晶体的熔沸点较低,氯化铝的熔沸点较低,所以为分子晶体。
②铝原子和氯原子之间形成共价键,还形成一个配位键,其结构为
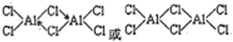 本题难度:一般
本题难度:一般
4、选择题 下列说法正确是???????????????????????????????????????????????????(???)
①所有基态原子核外电子排布都遵循构造原理
②同一周期从左到右,元素第一电离能、电负性都是越来越大
③所有化学键和氢键都具有相 同特征:方向性和饱和性
同特征:方向性和饱和性
④所有配合物都存在配位键,所有含配位键的化合物都是配合物
⑤所有含极 性键的分子都是极性分子
性键的分子都是极性分子
⑥所有离子晶体中都含有离子键
⑦所有金属晶体熔点肯定高于分子晶体
A.①②
B.⑥
C.③④⑤
D.①②⑥
参考答案:B
本题解析:略
本题难度:简单
5、选择题 关于下列几种离子晶体,说法不正确的是(???)
A.由于NaCl 晶体和CsCl晶体中正负离子半径比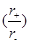 不相等,所以两晶体中离子的配位数不相等
不相等,所以两晶体中离子的配位数不相等
B.CaF2晶体中,Ca2+配位数为8,F-配位数为4不相等,主要是由于F-、Ca2+电荷(绝对值)不相同
C.MgO的熔点比MgCl2高主要是因为MgO的晶体能比MgCl2大
D.MCO3中M2+半径越大,MCO3热分解温度越低
参考答案:D
本题解析:A、正确,氯化钠配位数为6,氯化铯的配位数为8;
B、是由于电荷不相同引起的,正确。
C、离子晶体,电荷越多,半径越小,晶格能越大;
D、熔沸点与分解温度不是一回事。错误
本题难度:一般