微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各组混合物中,能用分液漏斗进行分离的是( )
A.苯和食盐水
B.碘和四氯化碳
C.酒精和水
D.食醋和水
参考答案:分液漏斗用于分离互不相溶的液体,题中B、C、D互溶,不能用分
本题解析:
本题难度:一般
2、选择题 为提纯下列物质(括号内为杂质)选用的试剂和分离方法都正确的是
?
| 物质
| 试剂
| 分离方法
|
①
| 硝酸钾(氯化钠)
| 蒸馏水
| 降温结晶
|
②
| 二氧化碳(氯化氢)
| 饱和碳酸钠溶液
| 洗气
|
③
| 乙醇(水)
| 金属钠
| 蒸馏
|
④
| NaCl溶液(Na2S)
| AgCl
| 过滤
A.①③????????B.①④???????C.只有②????????D.③④
参考答案:B
本题解析:
试题分析:①硝酸钾混有氯化钠,氯化钠溶解度随温度变化不大,硝酸钾溶解度随温度升高增大,利用冷却热饱和溶液的方法得到硝酸钾晶体;故①正确;②二氧化碳和碳酸钠溶液也发生反应,应该用饱和碳酸氢钠溶液除去CO2中的氯化氢气体,故②错误;③乙醇和水都和钠发生反应,不能除去水,应该利用新制生石灰借助于蒸馏除去乙醇中的水,故③错误;④加入氯化银是难溶物,但硫化银更难溶,可以和硫化钠反应实现沉淀转化Na2S+2AgCl=Ag2S+2NaCl,乙醇可以实现除杂,故④正确,答案选B。
本题难度:一般
3、实验题 (6分)A、B、C、D四种可溶性化合物,分别由阳离子Fe3+、Ba2+、Al3+、Na+和阴离子OH-、SO42-、Cl-、CO32-中的各一种组成(离子不重复)。通过实验,得出如下结论:
①A和D的溶液显碱性,0.1mol・L-1A溶液的pH小于13;
②铜粉能溶解在B的溶液中;
③往C的溶液中加入过量的D溶液,最终没有沉淀。
根据以上实验事实,回答下列问题:
(1) 试写出A和B的化学式:A?????????,B___________。
(2) 试写出实验③中反应的离子方程式??????????????????。
参考答案:(1) Na2CO3,Fe2(SO4)3。(2) Al3+
本题解析:
试题分析:A、B、C、D四种可溶性化合物,分别由阳离子Fe3+、Ba2+、Al3+、Na+和阴离子OH-、SO42-、Cl-、CO32-中的各一种组成(离子不重复)。①A和D的溶液显碱性,0.1mol・L-1A溶液的pH小于13,则A为碳酸钠,D为氢氧化钡;②铜粉能溶解在B的溶液中,则B为硫酸铁;③往C的溶液中加入过量的D溶液,最终没有沉淀,则C为氯化铝。(1)A和B的化学式:A:Na2CO3,B:Fe2(SO4)3。(2) 氯化铝与过量氢氧化钡反应的离子方程式为Al3+ + 4OH-====AlO2- + 2H2O。
本题难度:一般
4、选择题 化学反应a?A+b?B=d?D+e?E,已知40克A和21克B恰好完全反应生成28克D,则B、E两种物质的摩尔质量之比是
A.:
B.:
C.:
D.:
参考答案:D
本题解析:分析:依据质量守恒定律,求出E的质量,再根据化学反应中C和D的质量关系求出B、E两种物质的摩尔质量.
解答:生成物E的质量为40g+21g-28g=33g,
根据化学方程式a A+b?B=d?D+e?E,
??????????????????bM(B)??? e M(E)
????????????????? 21g????????? 33g
?则 , ,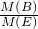 = = : :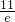 , ,
故选D.
点评:本题主要考查了化学计算,解此题的关键是要知道利用方程式找各物质的质量关系时摩尔质量需要乘以化学计量数.
本题难度:一般
5、选择题 下列混合物分离(或除杂)的方法不正确的是( )
A.用酒精可以从碘水中萃取碘
B.Fe(OH)3中含有少量Al(OH)3可用NaOH除去
C.NaCl中混有难溶于水的杂质可用溶解、过滤、蒸发、结晶的方法分离
D.Na2CO3中含有少量NaHCO3可用加热的方法提纯
参考答案:A
本题解析:
本题难度:简单
|