微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用光洁的铂丝蘸取无色溶液,在无色灯焰上灼烧时观察到黄色火焰,则下列叙述正确的是
A.只含钠离子
B.一定含钠离子,可能含钾离子
C.钠离子钾离子均有
D.可能含钠离子或钾离子中的一种
参考答案:B
本题解析:
本题难度:一般
2、选择题 已知在常温下,测得浓度均为0.1?mol/L的下列六种溶液的pH
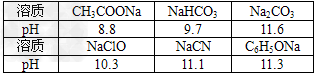
复分解反应存在一个规律:碱性较强的物质发生类似反应可以生成碱性较弱的物质。依照该规律,请你判断下列离子反应不能成立的是[???? ]
A.CO32-+C6H5OH→HCO3-+C6H5O-
B.CO2+H2O+ClO-===HCO3-+HClO
C.CO2+H2O+C6H5O-→HCO3-+C6H5OH
D.CO2+H2O+2C6H5O-→CO32-+2C6H5OH
参考答案:D
本题解析:
本题难度:一般
3、选择题 下列电离方程式正确的是(???)
A.NaHSO4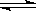 Na++H++SO42一
Na++H++SO42一
B.NaHCO3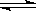 Na++ HCO3一
Na++ HCO3一
C.H2S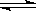 2H++S2-
2H++S2-
D.Mg(OH)2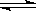 Mg2++2OH-
Mg2++2OH-
参考答案:D
本题解析:
试题分析:用化学式和离子符号表示电离过程的式子,称为电离方程式,表示物质溶解于水时电离成离子的化学方程式。硫酸氢钠、碳酸氢钠是强电解质,应该用等号,AB不正确;H2S是二元弱酸,电离是分步进行的,C不正确,答案选D。
点评:该题是高考中的常见考点,属于基础性试题的考查,难度不大。该题的关键是准确判断出电解质的强弱,然后具体问题、具体分析即可。
本题难度:简单
4、选择题 某由离子化合物组成的混合物只可能含有以下离子中的若干种:K+、NH4+、Mg2+、Ba2+、Cl-、CO32-、SO42-。为确定其组成,准确称取14.82g混合物溶于水得300 mL澄清溶液,分成三等份分别进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液并加热,经碱石灰干燥后收集到标况下气体1.12L
(3)第三份加足量BaCl2溶液,沉淀经洗涤、干燥后称重为6.27g,再向沉淀中加足量盐酸,经过滤、洗涤、干燥后称重为2.33 g
根据上述实验,以下推测不正确的是
A.溶液中c(SO42-)为0.1mol/L、c(CO32-) 为0.2mol/L
B.该混合物中不含Ba2+、Mg2+
C.一定存在NH4+、 K+,无法确定Cl-是否存在
D.实验(3)沉淀中加盐酸后,若只过滤、不洗涤,会对除NH4+外的其他离子含量的测定造成影响
参考答案:A
本题解析:
试题分析:①与AgNO3溶液有沉淀产生的离子有Cl-、CO32-、SO42-;②加足量NaOH溶液加热产生气体,气体是氨气,故一定有铵离子0.04mol;③不溶于盐酸的2.33g为硫酸钡,物质的量是0.01mol;6.27g沉淀是硫酸钡和碳酸钡,碳酸钡质量为6.27g-2.33g=3.94g,物质的量为0.02mol,故一定存在CO32-、SO42-,因而一定没有 Mg2+、Ba2+;c(CO32-)=0.02÷0.1=0.02(mol/L),再根据电荷守恒,正电荷为:n(+)=n(NH4+)=0
本题难度:一般
5、选择题 下列物质中属于非电解质的是:
A.氯化钾的水溶液
B.液态氯化氢
C.气态甲烷
D.作电极的碳棒
参考答案:C
本题解析:A错误,氯化钾的水溶液是混合物,不属于电解质,也不属于非电解质。
B错误,氯化氢是电解质。
C正确,属于非电解质。
D错误,碳棒是单质,不属于电解质,也不属于非电解质。所以正确答案选C。
本题难度:一般